2024银屑病生物制剂市场展望报告
1:银屑病是T细胞介导的自身免疫疾病
银屑病PsO:疾病介绍
银屑病是一种持久且反复发作的炎症性皮肤病,且与多种合并症发生相关。银屑病(Psoriasis,PsO)是一种由遗传、免疫及感染等多种因素诱发的慢性自身免疫性皮肤疾病,俗称“牛皮藓”,病程较长且易复发。《银屑病治疗靶点及其药物研发进展》提及该病在性别间发病率无异,且遗传为最重要的因素之一,约1/3的银屑病患者患有家族史,环境因素如压力、创伤、干扰等可能导致或加重疾病的发生。银屑病主要特征是皮肤上出现凸起的红色斑块,上面覆盖着银色的鳞屑,其组织学特征包括皮肤表层厚度增加、皮肤真皮内血管增生以及真皮内存在炎症细胞。《银屑病发病机制及药物调控研究进展》中指出国内银屑病发病率约为0.4%,欧美国家发病率更高达2-3%,且呈一定上升机制。此外银屑病不仅是一种皮肤病,还与多种合并症发生相关,如银屑病关节炎(PsA)、代谢综合征、心血管疾病和精神疾病。
银屑病发病机制:活化的T淋巴细胞在疾病进展中发挥着重要作用
功能性失调的辅助性T细胞(Th1、Th17、Th22和Treg细胞)是银屑病发生过程中不可或缺的因素。辅助性T细胞介导银屑病进展的发病机理在于,当受到某些触发因素(如感染或身体损伤等)刺激时,树突状细胞(DendriticCells,DC)可释放促炎因子,这些细胞因子激活CD4+T细胞增殖并极化成不同的辅助T细胞亚群,并产生许多细胞因子(如TNF-α、INF-γ、IL17和IL22)作用于角质形成细胞,放大银屑病炎症。
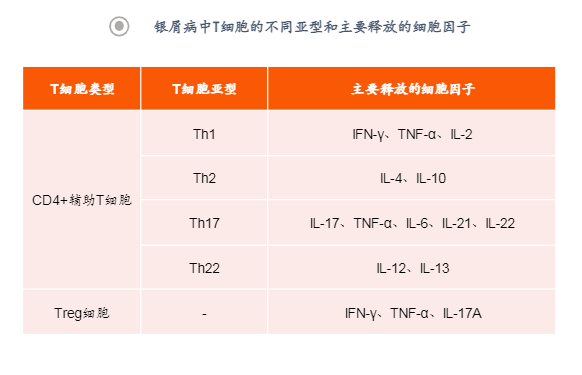
银屑病发病机制:TNF-α/IL-23/Th17轴
TNF-α是一种前炎症因子,在炎症反应的分子机制中处于上游地位。能作用于T淋巴细胞和巨噬细胞,使炎症因子如IL-1、IL-6、IL-8和趋化因子分泌增加,促进炎症反应的发生;此外TNF-α可以影响内皮细胞使黏附分子和血管内皮生长因子(VEGF)表达上调,导致炎症细胞浸润增加和血管生成,从而加剧炎症反应。炎症反应IL-23/Th17轴下游传导:①促炎因子TGF-β、IL-6、IL-1β的存在诱导幼稚CD4+T细胞向Th17细胞的初始分化,并导致Th17细胞表面IL-23R表达上调(IL-23信号转导所需);②树突状细胞和抗原呈递细胞释放的IL-23连接Th17细胞表面受体,激活和刺激Th17亚群细胞扩增,活化的Th17细胞诱导细胞因子IL-17A-F、IL-22、IL-21和TNF-α的产生;③IL-17A作用为刺激中性粒细胞募集和激活、直接激活角质细胞等,并与TNF-α协同增强炎症;IL-22诱导角质形成细胞过度增殖,与银屑病严重程度相关;IL-17A和IL-22是皮肤炎症的关键介质,最终导致银屑病的发生。
银屑病:分型及严重程度分级
银屑病分型:包括寻常型、脓疱型、红皮病型、银屑病关节炎(PsA)及其他特殊类型银屑病。最常见的银屑病类型是寻常型斑块状银屑病,主要表现皮肤和关节上干燥、界限分明、凸起的红色皮损,并伴有银色鳞屑,占所有银屑病病例80-90%。银屑病严重程度分级一般根据BSA、PASI即DLQI划分为轻中重度三级。银屑病通常根据体表面积(BSA,单个手掌及手指屈侧面积定义为人体表面积的1%,即评估患者全身皮损总和达到多少个手掌面积) 和银屑病面积和严重程度指数(PASI) 等测量结果分为轻度、中度和重度。为了避免低估疾病的严重程度,皮肤科医生还应考虑生活质量评估(例如皮肤科生活质量指数-DLQI)、既往治疗反应、“特殊区域”的受累情况(例如面部、头皮、手掌、脚底和生殖器)以及是否存在合并症。
银屑病:国内患者群体数量及市场规模
国内银屑病市场规模预计2025年超过200亿元,生物制剂用药占比逐年提升。据沙利文数据中国银屑病药物市场由2018年6.04亿美元快速增长至2022年14.36亿美元,复合年增长率为24.2%,预计2025年将达到32.55亿美元,2022年至2025年复合年增长率为31.4%。国内银屑病市场规模增长主要归因于:(1)银屑病药物市场生物制剂渗透率提升;(2)治疗银屑病生物制剂逐步纳入医保价格下降,改善患者对药物的负担能力,进一步推动药物市场的增长;(3)国内银屑病患者人群数量逐年增长,从2017年约650万人增至2022年约670万人,预计2030年将达到680万左右,其中20-30%患者患有中重度银屑病;(4)企业端营销力度加大,进一步扩大生物制剂在国内银屑病药物市场的覆盖,2022年生物制剂用药规模占整体银屑病药物规模约43.4%,预计2030年将上升至56.8%。
2:银屑病生物制剂:TNF-α/IL-23/IL-17全球及国内用药概况
银屑病:国内诊疗指南及生物制剂使用原则
目前银屑病是不可根治性疾病,选择适合患者的治疗药物和方法,对控制病情、减少共病、维持长期疗效、全面提高患者生活质量十分重要。考虑到银屑病的复杂性,治疗方案应根据患者病情个体化制订,轻度以外用治疗为主,中重度应系统治疗,对于传统系统药物治疗效果欠佳的患者可选择生物制剂或小分子药物治疗。生物制剂的使用原则:目前生物制剂在国内获批的适应症均为中重度斑块状银屑病,当患者病情需要接受系统治疗时,特别是接受光疗或传统系统治疗无效、失效或无法耐受且生物质量受到明显影响时,可考虑使用生物制剂。此外PsA对患者生物质量影响大,不及时控制有可能致畸、致残,建议积极考虑应用生物制剂;脓疱型和红皮病型银屑病如需使用生物制剂,可根据患者具体情况综合评估
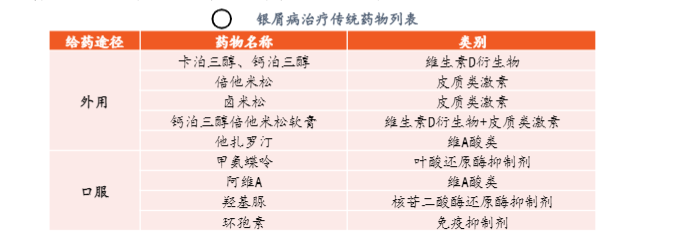
银屑病传统治疗药物
银屑病的早期研究重点是表皮增生,因而银屑病传统治疗药物主要目的是抑制表皮增生和抗炎。抑制表皮增生药物主要作用均是抑制细胞增殖:主要包括甲氨蝶呤、羟基脲、维生素D衍生物、维A酸类等,其中甲氨蝶呤和羟基脲是通过减少DNA复制而抑制细胞增殖,达到治疗银屑病的目的;维A酸类药物(主要有阿维A和他扎罗汀)和维生素D衍生物(主要有卡泊三醇和钙泊三醇)通过与表皮细胞相关受体结合,减少细胞因子诱导的T细胞增殖,同时维A酸类药物和维生素D衍生物还具有促进表皮分化等作用,对银屑病治疗具有一定优势。皮质类激素治疗主要目的是抗炎:外用皮质类激素主要包括倍他米松和卤米松,可单独进行局部给药或联合其他药物进行局部给药。环孢素主要原理是免疫抑制:环孢素是一种通过抑制T细胞活化和细胞因子表达的免疫抑制剂,环孢素的使用让学者对银屑病的发病机制有了更新的认识,即银屑病可能是一种T细胞调节功能异常的免疫性疾病。
生物制剂治疗银屑病数据对比(头对头)
结论:(1)TNF-α几款药物对比来看,头对头数据中依那西普疗效低于英夫利西单抗,而英夫利西单抗是人鼠嵌合单抗,是TNF-α中唯一需要静脉注射的药物,阿达木单抗皮下给药,非头对头英夫利西单抗数据来看,两者疗效相当;(2)IL-23是IL-17的上游信号,IL-17生物制剂临床起效快,而IL-23持续时间相对更长;(3)IL-23和IL-12共享p40亚基,靶向p40亚基相对而言对IL-23的定位不够精准,疗效略低。从头对头数据来看,IL-12/23p40代表药物乌司奴单抗头对头IL-17两款代表药物(司库奇尤单抗和依奇珠单抗),第12周乌司奴单抗PASI75和PASI90比例均低于司库奇尤单抗和依奇珠单抗;(4)第二代靶向IL-23抑制剂精准靶向IL-23独有p19亚基,代表药物为强生古塞奇尤单抗,48周头对头司库奇尤单抗数据,PASI90比例分别为84%vs70%。
司库奇尤单抗(可善挺):国内核心序列专利2025年到期,国内生物类似药进度靠前为百奥泰BAT2306,目前处于临床III期阶段;依奇珠单抗(拓咨):国内核心序列专利2026年到期;乌司奴单抗(喜达诺):国内氨基酸序列专利2021年8月到期,美国及欧洲专利分别于2023年9月及2024年1月到期,生物类似药国内进度靠前的为华东医药与荃信生物合作开发的QX001S,国内申请上市阶段;古塞奇尤单抗(特诺雅):国内专利期至2026年12月。
在52周临床III期试验中,可善挺(150mg或300mg)与安慰剂对比,治疗中国亚人群组中重度斑块状银屑病疗效和安全性均表现出优效。该试验共入组441名国内患者,被随机分配至三个治疗组:可善挺300mg(n=221)、150mg(n=110)、安慰剂组(n=110),主要终点为第12周IGA0/1和PASI75,次要终点为第12周PASI90。试验结果表明第12周可善挺300mg、150mg与安慰剂组达到IGA0/1的比例分别为82.3%、69.7%和2.7%,第12周达到PASI75的比例分别为97.7%、87.2%和3.7%,第12周PASI90比例分别为81%、65.7%和0.9%,且治疗疗效一直延续至52周,从12周至52周,可善挺300mg和150mg组的PASI100反应持续增加,300mg可善挺第12周与52周PASI100缓解率分别为32.9%vs42.1%,150mg药物治疗12周和52周PASI100缓解率分别为20%vs32.5%。
2021年4月拓咨(依奇珠单抗)国内成人中重度银屑病临床III期(RHBH)试验完成,主要终点是评估第12周拓咨80mg每2周1次、80mg每4周1次sPGA0/1(静态医师总体评估)和PASI75比例,此外第12周后随机分配维持给药期至第60周以评估长期安全性及有效性。结果表明第12周,拓咨80mgQ2W组86.4%患者达到sPGA(0,1),93.8%患者达到PASI75,82.4%患者达到PASI90,33%患者达到PASI100,此外维持给药组患者高应答持续维持至60周。在起效时间方面,第1周拓咨80mgQ2W组PASI50应答率即显著高于安慰剂组,第2周,拓咨80mgQ2W组PASI75和sPGA(0,1)应答率显著高于安慰剂组。安全性上拓咨在中国患者耐受性良好。
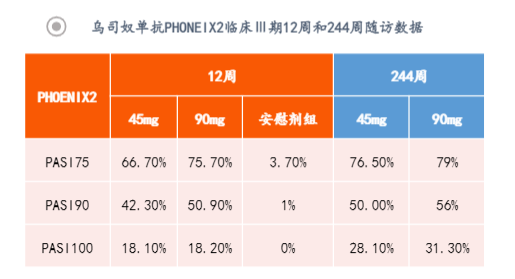
喜达诺(IL-12/23p40):5年随访结果表明对中重度PsO患者长期疗效和安全性
喜达诺(IL-12/23p40):5年随访结果表明对中重度PsO患者长期疗效和安全性长期疗效数据:乌司奴单抗(喜达诺)通过与IL-12和IL-23所共有的p40蛋白亚单位高亲和力特异性结合,从而抑制银屑病的发展。其PHOENIX1和PHONENIX2两项涉及1996例患者的随机双盲安慰剂对照III期结果表明喜达诺长期疗效持久,维持皮损清除及生活质量改善可达5年。此外真实世界研究证实乌司奴单抗的药物留存率高于TNF抑制剂和IL-17抑制剂,药物留存率高可以反映乌司奴单抗具有良好的长期有效性及安全性。中国人群的LOTUS临床三期试验:患者(n=332)随机接受喜达诺45mg或安慰剂治疗,在12周时使用安慰剂患者转换为乌司奴单抗45mg并随访至28周。结果表明接受喜达诺45mg治疗12周,82.5%达到主要临床终点PASI75,安慰剂组为11.1%。其后在24周达到峰值(PASI75、PASI90和PGA0/1分别为91.6%、79.9%、85.1%),并一直维持至28周(PASI75、PASI90和PGA0/1分别为91.5%、80.4%、85.8%)。
特诺雅(IL-23p19):“延缓复发”和“皮损全面清除”治疗银屑病目标
古塞奇尤单抗(特诺雅)是国内首个靶向IL-23p19亚基抑制剂,在针对中重度斑块状银屑病的两项关键研究(VOYAGE1和VOYAGE2)中,特诺雅已被证明在第16周疗效优于安慰剂和TNF-α抑制剂阿达木单抗;且在头对头司库奇尤单抗临床III期试验中,48周特诺雅组PASI90比例为84%,而司库奇尤单抗组PASI90比例为70%。此外特诺雅两项III期5年随访结果表明其疗效持久,第252周PASI在VOYAGE1和VOYAGE2试验均达到80%以上,PASI100比例达到一半以上。
从国内样本医院销售数据来看,可善挺院端销售体量居银屑病生物制剂大头,2020年底可善挺进入医保后,2021年迅速放量;依奇珠单抗和乌司奴单抗国内2021年底进入医保,2022年样本医院销售额增速迅猛;古塞奇尤单抗2022进入国内医保,2023年3月开始执行,从2023年样本医院销售额来看,纳入医保对其放量同样有较大的提升促进作用。
国内IL-17在研进度靠前:(1)智翔金泰GR1501银屑病适应症于2023年3月上市获受理,恒瑞医药SHR-1314银屑病适应症于2023年4月上市获受理,预计两家于2024年相继国内上市;(2)三生国健SSGJ-608银屑病适应症于2023上半年完成III期入组,康方生物AK111银屑病2023下半年完成入组,预计两家于2024年完成临床III期;(3)预计2025年UCB比吉丽珠单抗、丽珠集团&鑫康合XKH004、君实生物JS005银屑病完成临床
国内IL-17在研进度靠前:(1)智翔金泰GR1501银屑病适应症于2023年3月上市获受理,恒瑞医药SHR-1314银屑病适应症于2023年4月上市获受理,预计两家于2024年相继国内上市;(2)三生国健SSGJ-608银屑病适应症于2023上半年完成III期入组,康方生物AK111银屑病2023下半年完成入组,预计两家于2024年完成临床III期;(3)预计2025年UCB比吉丽珠单抗、丽珠集团&鑫康合XKH004、君实生物JS005银屑病完成临床
3:投资建议:关注管线进度靠前,具备先发优势的企业
投资建议:关注管线进展靠前,具备先发优势的企业
银屑病是一种病程长易复发的自免性疾病,国内患病人群在600-700万之间,2022年国内用药市场规模约100亿元,远期2030年预计达400亿元左右。对银屑病发病机制深入研究结果表明活化的T淋巴细胞在疾病进展发挥关键作用,其中IL-23/IL-17为炎症传导的关键因子,建议关注几大方向:①国内生物类似药在研:进度靠前的为乌司奴单抗生物类似药(华东医药&荃信生物-申请上市,百奥泰-临床III期,石药集团-临床III期),司库奇尤单抗生物类似药(百奥泰-临床III期);②IL-17在研:预计2024年智翔金泰GR1501和恒瑞医药SHR-1314国内上市,2025年三生国健SSGJ-608和康方生物AK111完成临床III期,2026年丽珠集团XKH004,君实生物JS005完成临床III期;③IL-23在研:康方生物AK101申请上市中,信达生物IBI-112临床III期。
风险提示
行业政策变动风险:医药行业受到国家及各级地方药品监督管理部门和卫生部门等监管部门的严格监管。随着国家医疗卫生体制改革的不断深入和社会医疗保障体制的逐步完善,行业政策环境可能面临重大变化。研发进展不及预期风险:新药研发包括药物的新药发现、临床前研究和开发、新药临床试验申请、临床I-III期试验开发、新药上市申请及上市后研究等多个环节,创新药研发难度大,存在研发进展不及预期风险。竞争加剧风险:新药的研发和商业化领域竞争激烈,未来随着更多企业药物产品陆续获批上市,市场竞争格局加剧,进而对行业规模产生不利影响等。产品上市后商业化表现不及预期:新药研发成功获批后,还需要经历市场拓展与学术推广,才能够更广泛地被医生和患者所接受,在新药市场教育初期阶段,医生或患者不了解产品特点,导致产品销售不达预期等。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)