2024医药行业投资策略报告
1.医疗器械:出海势在必行
随着国产器械厂家产品力和品牌力逐步提升,国内市场日益成熟,出海成为未来国内医疗器械厂商的发展主线。
1.1全球医疗器械市场空间广阔
发达国家展现较高的消费水平,部分发展中国家具备较大消费潜力。美国、日本、德国、英国、法国、加拿大、意大利、韩国、西班牙和巴西等国家位列全球前50,显示出其庞大的市场和国民的高消费水平。同时印度、中国、印度尼西亚等国家虽然人均GDP排名未进入前50,但GDP总量和增速均表现强劲,预示着它们作为未来潜在的新兴市场具有较大的发展潜力。欧美处于成熟市场,亚太和拉丁美洲处于快速发展阶段。根据IQVIA数据,2021年全球医疗器械市场规模为6,108亿美元,预计2025年达到7,667亿美元,年复合增速为5.9%。其中北美洲市场规模最大,2021年达2099亿美元,但增速有所放缓,2021-2025年CAGR为4%。亚太为新兴快速发展市场,2021年亚太市场空间为1502亿美元,2021-2025年CAGR为9%,高于全球平均水平。
2021年市场空间前三的国家为美国、中国和德国,增速前三的国家是印度(12.6%)、中国(10.6%)和哥伦比亚(10.0%)。未来随着老龄化程度加剧、治疗需求提升等,市场空间有望进一步扩容。2022年全球医疗器械市场中,美国份额占比最高,达34%,其次为中国和德国。
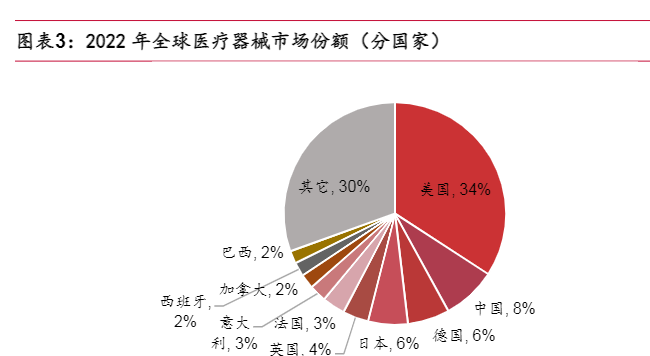
美国公司在全球医疗器械领域占据领先地位,日本和德国紧随其后。2023年全球医疗器械营收前50名公司中,美国有27家,总营收达2980亿美元,其次为日本(7家)和德国(3家)。
全球营收TOP100医疗器械公司中中国公司数逐步增加。2023年全球营收TOP100医疗器械公司中美国占比最高,达到47%,其次为中国(18%)和日本(16%)。2010-2023年期间中国医疗器械公司在全球营收TOP100的占比有所提升,从2010年的14%提升至2023年的18%,持续赶超日本和欧盟。中国医疗器械公司逐步跻身全球中高端市场。2023年全球营收前30名医疗器械公司中,中国有迈瑞医疗。此前2010年和2015年均未有中国医疗器械公司进入全球营收前30名,说明中国产品逐步获得全球中高端市场认可。同时中国公司在全球中端市场(指公司营收进入全球第61-90名)的比例逐步提升,从2010年的6%提升至2023年的11%。
1.2医疗器械出海快速发展
我国医疗器械出口额占总出口额比例逐步提升,2017-2019年期间从0.44%提升至0.52%。新冠疫情期间,我国医疗器械产品出口大幅提升,2020年我国医疗器械出口额占总出口额达到0.70%,之后随着新冠相关产品需求下滑,我国医疗器械出口额有所回落,占总出口额比例稳定在0.6%左右。
从整体来看,中国医疗器械出口增速快于总体出口。2017-2019年期间,我国医疗器械出口金额年复合增速为13.30%,高于总体出口(5.09%)。凭借优良稳定的供货和高性价比产品优势,2020年中国医疗器械出口额大幅提升,同比增长40.45%,全球知名度进一步得到提升。2021-2022年受高库存、需求减少影响,我国医疗器械出口疲软。2024年以来中国医疗器械出口额呈现弱复苏态势,反映海外需求逐步提升,未来有望适度加快。
股医疗器械海外营收占总医疗器械出口额比例逐步提升。2017年A股医疗器械公司海外营收为34亿美元,占总体医疗器械出口额比例为34%。新冠疫情期间,与检测相关的器械公司上市速度加快,截至2023年底,A股医疗器械公司海外营收达96亿美元,与2017年相比提升2.8倍,占总医疗器械出口额比例达52%。
1.3出海品种由中低端逐步转为中高端
回顾2019-2023年医疗器械行业出海历史。受新冠疫情影响,2020-2022年期间中国医疗器械厂家凭借高性价比防疫产品和稳定供应能力,获得全球客户认可,海外营收占比得到快速提升,从2019年的25%提升至2022年的34%,而后回落至2023年的29%。中高端医疗设备出口呈现恢复性增长。2020-2022年与新冠检测相关的IVD板块出口获得较快增长。同时凭借新冠产品,中国快速打开在海外市场的知名度,带动中高端医疗设备的增长,2021-2023年医疗设备海外营收增速不断提升,2023年达10%,体现中国制造逐步得到全球认可。
2020-2023年中国医疗器械出口大幅增长,全球国际化水平逐步提升。2023年SW医疗器械公司共有124家,其中105家拥有海外营收。2017-2023年医疗器械公司海外营收年复合增速为18.53%,高于整体营收增速(13.93%)。2019年,国内医疗器械海外收入前十大公司中,包括低值耗材类公司5家,出口品种包括手套、口罩、纱布等;家用、康复类设备公司两家,例如家用呼吸机、血糖仪等,仅有迈瑞一家以常规医疗器械为主,例如监护仪、血球分析仪、超声等。2023年医疗器械出口前十位厂家涉及品种逐步丰富,包括血糖仪、制药装备、大型影像设备等,均有较为亮眼出口表现。随着全球逐步从疫情恢复,常规医疗器械需求不断提升,我们认为对于以常规医疗器械为主导的国内厂家是利好。
结合医疗器械申万三级子行业出口占比,以及上述医疗器械出口前十厂家涉及品种,我们认为目前国内厂家出海销售的设备可以分成三大类:低值耗材、中高端器械和全球领先创新。低值耗材类产品包括手套、口罩等低值耗材,以及胶体金检测试剂盒等成熟检测产品,国内技术成熟,规模化生产优势使得产品价格处于全球领先位置,也是目前国内医疗器械主要出口品种。主要风险在于其他发展中国家,以更低的加工成本进行竞争,或者劣币驱逐良币,通过质量较差但价格更优的产品进行恶性竞争。中高端器械产品种类较多,涉及厂家类型多样,包括体外诊断、影像、康复、部分耗材类公司,我们认为中短期仍是国内医疗器械厂家海外高速增长的品种,以迈瑞医疗、万孚生物为代表的厂家,通过以丰富的产品类型进入各个国家/区域,满足不同客户需求,复制进口品牌过去发展轨迹。因为单个产品涉及品类较多,各个国家准入规则不同,对于厂家资源投入要求较高。全球领先创新类产品在国内外都处于行业发展阶段,产品渗透率仍有较大提升空间,也是进口器械品牌主要把控的领域,随着进入这一领域,意味着要与全球头部厂家直面竞争,同时地缘政治风险影响不确定性较大。
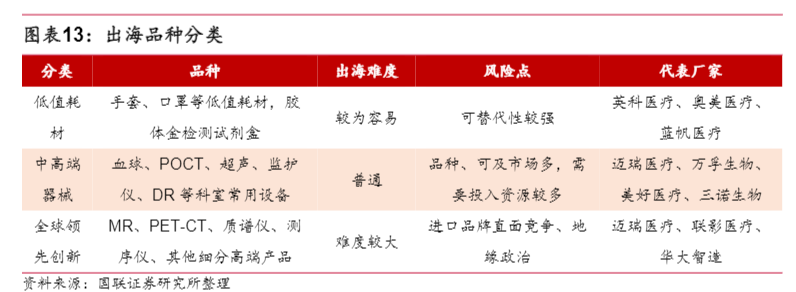
综合目前国内厂家发展阶段,我们认为中短期仍然以低值耗材类和中高端器械为主,头部厂家通过早期的耕耘,已经进入的国家和区域数量有明显优势,包括注册还有渠道的建设都形成门槛,同时潜在的受众群体较大,仍然主要受益于厂家和品种。随着全球医疗水平的不断提升,现阶段处于进阶类的产品,也有望逐步普及,在中长期成为基础类产品,使得全球更多用户受益。
2.药品:高质量创新成主旋律
2.1国内政策鼓励高质量创新药研发
进入2024年以来,国家相继出台了《关于建立新上市化学药品首发价格形成机制鼓励高质量创新的通知(征求意见稿)》(以下简称“创新药首发定价征求意见稿”)和《深化医药卫生体制改革2024年重点工作任务》。包括北京、广州在内的各省市也相继发布了地方的创新药械全链条支持政策,充分体现了国家对研发具备自主知识产权的高质量创新药的高度重视。
全国医保基金充裕的年度累计结余金额也从支付端为未来鼓励和支持高质量创新药的研发和销售提供了有力保障。创新药首发定价征求意见稿鼓励高质量药品创新为进一步落实企业自主制定药品价格政策要求,鼓励以临床价值为导向的药物研发创新,支持高质量创新药品的多元供给和公平可及,充分发挥市场决定性作用,更好发挥政府作用,健全药品价格形成机制,2024年2月5日国家医保局发布《关于建立新上市化学药品首发价格形成机制鼓励高质量创新的通知(征求意见稿)》,拟要求药企从药学、临床价值和循证证据三方面对药品创新程度进行自评,按照自评点数将首次进入国内医药采购市场销售的新上市化学药品划分为高、中、低三档。自评点数高和居中的新上市药品,赋予首发价格1~5年不等的稳定期。稳定期内不纳入集中带量采购范围,不实施政府定价或政府指导价,暂不以当地挂网规则要求降价,不与国外价格作比较。此征求意见稿充分体现了政府对高质量创新药品的高度认可,通过分层次、有差别的价格措施,支持有临床价值的高质量创新,并挂网、采购等关键政策资源重点分配给真正具有创新性、高水平创新的企业。创新药械全链条支持政策有望进一步落地2024年4月,北京、广州、珠海、海口等城市相继出台并推动创新药全链条政策落地,对创新药研发、审批及支付方式等全链条环节进行多维度赋能。
以北京为例,着重针对1)提升创新药临床研究质量和效率;2)优化创新药审评审批机制;3)加快创新药配备使用;4)提高创新药多元支付能力;5)医疗健康数据赋能创新;6)强化创新医药企业投融资支持等多个方面出台了相关鼓励政策。2024年6月3日,国务院办公厅印发《深化医药卫生体制改革2024年重点工作任务》。在深化药品审评审批制度改革内容部分,明确提出要制定关于全链条支持创新药发展的指导性文件。加快创新药、罕见病治疗药品、临床急需药品等以及创新医疗器械、疫情防控药械审评审批。医保基金创新药支付能力充裕2023年全国医保基金累计结余超4.7万亿元,具备充裕的支付能力支持创新。2022年医保为创新药支付481亿元,占比当年收入不到2%,参考欧美发达国家创新药支付占比创新药行业具备较大成长空间。
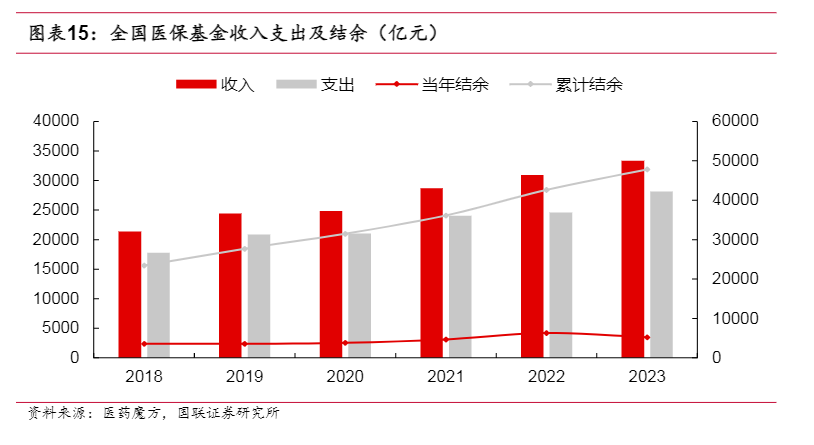
2.2原创性药品出海获得充分溢价
考虑到欧美市场在药品市场定价(国内有医保谈判)、支付端买单能力与意愿(国内医保参保基数大、支付体系改革等)上的差异,国内药企为了1)能够在短期内实现资金回笼,尽快推进后续研发动作;2)通过跨国药企(MNC)的站台背书快速获得资本市场认可,加速融资,实现进一步“回血”;3)在“高投入、高风险”后实现“高回报”等原因也会选择主动出海,推动自研药物产品进入定价更高、支付体系更成熟的欧美市场。考虑到海外高昂的临床试验成本、以及与国内迥异的商业化环境,绝大部分国内药企不具备直接出海所需的海外临床和商业化能力,因此更多会采用门槛低、风险小的License out “借船出海”,即药企将自己已上市或在研产品的部分或全部权益售让给海外药企,借助海外药企的经验或渠道实现新药产品出海。通过这种合作方式可借助海外药企在研发端的丰富经验和资源实现优势互补、降低新药研发风险;同时通过合作方已搭建的成熟销售网络快速进入国际市场、获得丰厚现金流。
药品创新度决定出海交易金额2024年,中国药企达成的已披露金额的创新药出海交易已有13起。从披露信息来看,交易总金额已超161.27亿美元,首付款最高达到1.85亿美元(舶望制药4项核酸药物授权诺华)。从产品类型来看,药物授权出海集中在小分子(6起)和抗体(4起)。
2023年,中国药企达成的已披露金额的创新药出海交易已有27起。从披露信息来看,交易总金额已超346.61亿美元,首付款最高的是百利天恒EGFR/HER3双抗ADC产品BL-B01D1授权给百时美施贵宝(Bristol Myers Squibb,下文简称BMS)的8亿美元。从产品类型来看,药物授权出海集中在ADC产品(12起)和小分子药物(10起),其次是抗体药物(6起)和细胞治疗产品(1起)。
药品的潜在市场和创新程度对授权交易金额尤其是首付款有较大影响。在2023-2024年出海的药品中,首付款超过1.5亿美元的创新药均为潜在的FIC或BIC产品。参考国家医保局发布的“创新药首发定价征求意见稿”中对创新药的评分体系,我们认为可以主要从药学、临床价值和循证证据三个维度来评定药品的创新度:1)药学:以新机制、新靶点、新分子结构为优。以百利天恒授权给BMS的EGFR/HER3双抗ADC BL-B01D1为经典案例,在全球范围内首创了此类靶点组合的双抗ADC,同时已在肺癌、乳腺癌和鼻咽癌、头颈鳞癌等多个实体瘤适应症上初步验证了疗效,因此获得了破纪录的8亿美元首付款。相比来说,通过”Fast-follow”策略开发的潜在BIC产品,在授权出海时给的交易金额会相对低一些。2)临床价值:真正以临床价值为导向,填补未被满足的临床需求。获得CDE或FDA的突破性疗法认证是加分项。对引进方来说,引进的产品是否能够与自身擅长疾病领域或产品管线的战略布局具备较好匹配度和协同性,从而填补产品组合的空缺,会是比较重要的考量点。同样以百利天恒的BL-B01D1为例,作为一个潜在的可治疗肺癌、乳腺癌、食管癌、鼻咽癌等多个实体瘤的抗泛瘤种药物,同时可满足ADC+IO的联用逻辑,从而有望延长BMS的Opdivo药物的生命周期,自然容易获得青睐。3)循证证据:临床设计以有效为佳,等效设计好于非劣。
2.3关注FIC与BIC国产创新药
随着国内创新药企业在多特异性抗体、ADC等结构类型的靶点组合与工程学改造技术上日趋成熟,以及在产品靶点和适应症上的差异化布局,已涌现出越来越多的高质量创新药管线,并迎来了又一轮国产创新药出海热潮。我们预计创新药全产业链支持政策有望在全国进一步推进和落地实施,建议关注真正具备FIC或BIC潜力的国产创新药。2.3.1国产FIC与潜在FIC创新药中国创新药起步较晚、发展时间尚短,在靶点发现和转化医学上相对落后,能真正做出全球FIC的创新药尚属凤毛麟角。随着国内药企在CLDN18.2等靶点上的提前布局和在靶点组合上的持续深耕,有望涌现出多款具备全球FIC潜力的创新药。康方生物双抗药物领衔国产FIC创新药据国联证券研究所不完全统计,目前成功获批上市的全球FIC国产创新药主要有康方生物的两款双特异性抗体药物,包括靶向PD-1/CTLA-4的卡度尼利单抗(获批治疗既往接受含铂化疗治疗失败的复发或转移性宫颈癌)和靶向PD-1/VEGF的伊沃西单抗(获批联用化疗治疗EGFRTKI治疗后进展的EGFR突变局部晚期或转移性非鳞状非小细胞肺癌)。
ASCO 2024年度会议期间,康方生物披露了伊沃西单药对比帕博利珠单抗(K药)一线治疗PD-L1表达阳性(PD-L1 TPS≥1%)的局部晚期或转移性非小细胞肺癌(NSCLC)的HARMONi-2注册性III期临床研究数据,在意向治疗人群(ITT)中,依沃西组相较于K药组显著延长了患者无进展生存期(PFS),风险比(HR)显著优于预期,是全球首个且唯一在III期单药头对头临床研究中证明疗效显著优于K药的药物。除了康方生物已获批上市的两款双抗产品之外,已进入注册临床阶段、具备全球FIC潜力的国产创新药涵盖了单抗、双抗、ADC、CAR-T和小分子等药物结构类型,涉及的靶点包括CLDN18.2、B7H4、BTLA、SHP2、EGFR和靶点组合。CLDN18.2和ADC助力国产创新药兑现“FIC”潜力CLDN18.2靶向疗法开发进度全球领先。归因于胃癌在亚洲的高发病率,国内普遍早于欧美启动对CLDN18.2靶点的新药研究与开发,全球在研的132款CLDN18.2靶向药物中有108款国产药物,占比82%。单抗、双抗、ADC和CAR-T占据CLDN18.2靶向药物开发的主流,其中单抗和ADC进展相对较快。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)