2024钢铁信息化行业报告:智能制造新突破
1.技术底蕴丰富的ADC前沿创新药企
1.1管理层经验丰富打造创新平台优势
科伦博泰致力于创新药物的研发、制造及商业化,并作为抗体偶联药物(ADC)的先驱及领先开发公司之一。
1)2013-2015年技术积淀期,科伦药物研究生物中心和小分子研究中心分别成立,积淀技术底蕴,期间首款生物药抗EGFR单抗注射液A140成功申报临床;
2)2016-2022年打造梯队化临床管线,科伦博泰成立并推动多款产品进入临床阶段,2022年公司同默沙东就SKB-264、SKB-315及至多七项临床前ADC签订合作协议;
3)2023年至今,巩固优势并启动商业化布局,2023年公司成功上市,2024年预计部分优势产品将获批上市并正式启动商业化进程。
实控人技术出身,管理层经验丰富。董事长刘革新同为科伦药业创始人,具备丰富的产业管理经验,能够把控公司的管理及战略发展。此外,公司管理层深耕各细分领域多年,能够全流程把控新药从早期研发、临床开发到生产质量控制以及商业化布局。
科伦博泰在ADC领域积累了超10年的开发经验,作为中国首批建立一体化ADC研发平台OptiDC的生物制药公司之一。公司具备研发、生产、质量控制及商业化的一体化药物开发能力,已具备在ADC、大分子(单抗和双抗)以及小分子药物等方面的专有技术,并已被众多临床阶段候选药物所验证。
1.2管线频频出海验证产品临床价值
科伦博泰多款产品同默沙东深入合作。2018年,科伦博泰同和铂医药就泰瑞利单抗(PDL1)签订合作协议,最高总交易金额达3.57亿美元;2021年,科伦博泰同Ellipses就KL590586(RET抑制剂)签订合作协议;2022年,科伦博泰同默沙东就多款ADC产品签订3项合作协议,其中SKB-264(Trop2 ADC)最高总交易金额达14.10亿美元,SKB-315(CLDN18.2 ADC)最高总交易金额达9.36亿美元,7个在研ADC项目最高总交易金额达94.75亿美元。
科伦博泰现金储备迅速增长,研发投入始终保持在较高区间内。2021-2023年公司收入从0.32亿元增长至15.40亿元,CAGR 589%,主要源于默沙东支付的首付款及里程碑;期末现金储备从0.82亿元增长至15.29亿元;公司研发费用稳中有升,2021-2023年,研发费用从7.28亿元增长至10.31亿元,从而确保管线的持续推进。
科伦博泰聚焦肿瘤领域(乳腺癌、非小细胞肺癌以及胃肠癌等),并同时针对患者基数广泛的非肿瘤领域战略性推进临床管线。截至2024年5月,公司已拥有10余款处于临床阶段的候选药物,其中5款处于关键试验或NDA注册阶段。
2.全球高发癌种药物市场规模保持扩张
肺癌和乳腺癌作为全球高发癌种,患者基数广泛。全球范围内,乳腺癌、肺癌以及结直肠癌作为前三高发病种,2022年新发人数达235万人、233万人以及198万人。中国区域,肺癌、胃癌以及结直肠癌则作为前三高发病种,2022年新发人数达98万人、50万人以及48万人,其中乳腺癌新发人数达34万人。
2.1基因分型推动NSCLC靶向治疗愈发普及
非小细胞肺癌(NSCLC)作为最常见的肺癌类型,靶向药物市场规模保持快速增长。NSCLC发病率约占肺癌总数的85%左右,预计2030年,全球NSCLC患者的新发病例数达246万人,中国NSCLC患者的新发病例数达104万人。2017-2023年,全球NSCLC靶向药物市场规模从192亿美元增长至463亿美元,CAGR 15%;中国NSCLC靶向药物市场规模从11亿美元增长至78亿美元,CAGR 31%。
NSCLC生物标志物的出现推动患者进行靶向治疗。全球范围内,腺癌占比NSCLC病例总数的50-60%,腺癌中最常见的基因突变在NSCLC中占比分别为:KRAS 13%,EGFR激活突变9%,ALK 4%,MET扩增3%,MET外显子14可变2%;中国区域,常见的基因突变在NSCLC中占比分别为:EGFR 48%,KRAS 10%,ALK 5%。
根据CSCO指南,治疗方案主要针对不同驱动基因进行给药建议。针对EGFR敏感突变NSCLC,一线治疗主要使用EGFR TKI单药或联合化疗/贝伐珠单抗进行治疗,若EGFR TKI耐药后广泛进展则采用含铂双药化疗±贝伐珠单抗。若针对EGFR 20外显子插入突变NSCLC,后线治疗主要采用莫博赛替尼和埃万妥单抗。后续针对ROS1融合、BRAF V600E突变、NTRK等不同驱动基因NSCLC亚型则给出对应抑制剂给药方案。若针对无驱动基因NSCLC则主要使用化疗±贝伐珠单抗/PD-1/PD-L1。
2.1乳腺癌市场广阔末线靶向疗法欠缺
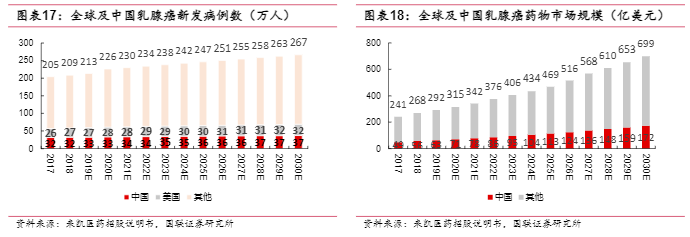
乳腺癌是全球女性最常见的癌症类型之一。预计2030年,全球和中国乳腺癌患者的新发病例数分别达267万人、37万人;全球和中国乳腺癌药物市场规模分别达699亿美元、172亿美元。根据激素受体(HR,包括雌激素受体ER及孕激素受体PR)及表皮生长因子-2(HER2)的表达水平区分乳腺癌亚型,其中全球乳腺癌HR+发病人数占比76.2%,HER2+占比20.2%,TNBC占比15%。
根据CSCO指南,针对HER2阳性晚期乳腺癌,若曲妥珠单抗治疗敏感则优先推荐紫杉类药物+曲妥珠单抗+帕妥珠单抗,或者紫杉类药物+曲妥珠单抗+TKI;若曲妥珠单抗治疗失败则主要推荐TKI+化疗,或者T-DM1(ADC)。针对TNBC,若紫杉醇类治疗敏感则优先推荐紫杉类药物单药或联合化疗。针对激素受体阳性晚期乳腺癌,优先推荐内分泌疗法联合CDK4/6抑制剂。
3.SKB-264:布局泛瘤种的ADC大单品
Trop2(Trophoblast cell-surface antigen 2,滋养层细胞表面抗原2)是一种具有临床价值的ADC靶点,在多种上皮癌中过度表达且异质性低。Trop2属于跨膜蛋白,由细胞外结构域、单个跨膜结构域和细胞内区域组成,在胚胎和器官发育中起重要作用,主要在上皮细胞中表达,正常组织中的表达较低。Trop2调节多种信号分子并参与致癌性相关信号通路,例如通过调节钙信号传导、细胞周期蛋白表达以及减少纤连蛋白粘附从而促进细胞生长、增殖和肿瘤转移。
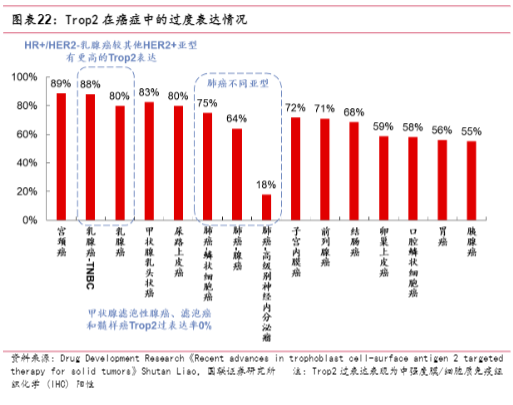
Trop-2在多种上皮癌中高度表达。Trop-2在80%的乳腺癌中过表达,其中TNBC的Trop-2过表达率高达88%;肺癌领域,75%的肺鳞状细胞癌、64%的肺腺癌以及18%的肺高级别神经内分泌肿瘤中观察到Trop-2过表达。此外,Trop-2在宫颈癌、甲状腺乳头状癌、尿路上皮癌以及子宫内膜癌等癌症中均呈现过表达状态。
3.1默沙东背书频频启动全球大三期临床
靶向Trop-2 ADC产品中,SKB-264具备“Best-in-Class”潜力,能够更好地平衡脱靶毒性和在靶脱瘤毒性。抗体端,SKB-264采用吉利德已经验证过的赛妥珠单抗;毒素端,SKB-264采用贝洛替康衍生物,毒性适中;Linker端,SKB-264采用含2-甲磺酰基嘧啶的CL2A连接子,血浆稳定性优于Trodelvy但差于DS-1062,因此脱靶毒性较Trodelvy更弱,而因为TROP-2靶点在粘膜等非肿瘤组织分布引起的口腔炎等,在靶脱瘤毒性则相对DS-1062更弱。
迄今为止,默沙东已启动9项全球多中心临床试验,针对肺癌适应症,MK-2870几乎覆盖从早期到末线的绝大部分NSCLC患者。
1)可切除II-IIIB期NSCLC:MK-2870-019研究主要评估MK-2870+帕博利珠单抗联合治疗vs帕博利珠单抗单药治疗在可切除II-IIIB期NSCLC中的疗效及安全性。
2)转移性NSCLC(1L治疗):MK-2870-007研究主要评估MK-2870+帕博利珠单抗联合治疗vs帕博利珠单抗针对PD-L1 TPS≥50%的转移性NSCLC患者疗效及安全性。MK-2870-023研究主要评估MK-2870+帕博利珠单抗+卡铂+紫杉醇vs帕博利珠单抗+卡铂+紫杉醇针对转移性鳞状非小细胞肺癌的患者一线治疗的疗效及安全性。
3)EGFR突变晚期非鳞状NSCLC(≥2L治疗):MK-2870-009研究主要评估MK-2870单药vs含铂双药化疗(培美曲塞+卡铂)在EGFR TKI耐药后非鳞状NSCLC患者中的疗效及安全性。
4)EGFR突变/其他基因突变非鳞状NSCLC(≥3L治疗):MK-2870-004研究主要评估MK-2870单药vs化疗(多西他赛、培美曲塞)在晚期伴基因突变的非鳞状NSCLC患者中的疗效及安全性。
除了肺癌适应症,MK-2870也针对既往经PD-1+化疗新辅助治疗术后未达到pCR的三阴乳腺癌、经内分泌治疗后进展的HR+/HER2-乳腺癌、末线晚期胃癌和末线子宫内膜癌进行了布局。
1)MK-2870-012入组人群为经PD-1+化疗新辅助治疗术后未达到pCR的三阴乳腺癌患者,主要将MK-2870+帕博利珠单抗vs 标准疗法进行比较。
2)MK-2870-010入组人群为经内分泌治疗后进展的HR+/HER2-乳腺癌患者,主要将MK-2870单药vs MK-2870+帕博利珠单抗联合治疗vs化疗药物进行对比。
3)MK-2870-015入组人群为治疗线数≥3L的晚期/转移性胃食管腺癌,该研究主要将MK-2870同标准疗法进行比较。
4)MK-2870-005入组人群为经铂类化疗+免疫治疗后的子宫内膜癌患者,主要将MK-2870同化疗药物进行对比。
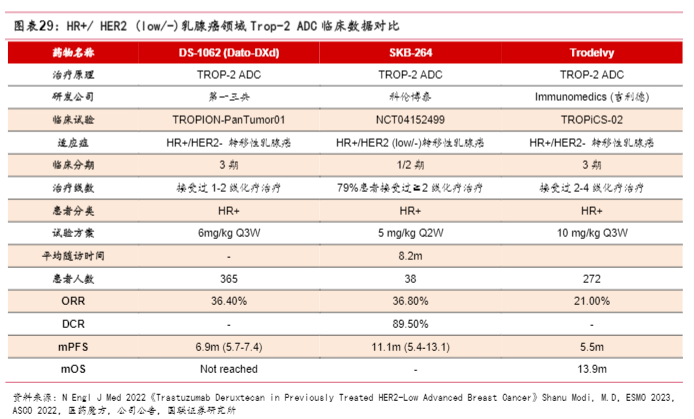
3.2SKB-264临床数据优越有望成为同类最佳
我们选取NSCLC末线领域具有代表性的3个创新疗法进行比较:SKB-264(Trop-2 ADC)、BL-B01D1(EGFR/HER3 ADC)、AK112(PD-1/VEGFα双抗)。
针对EGFR突变型NSCLC,Trop-2 ADC靶向疗法SKB-264 PFS疗效优越。SKB-264/AK-112分别入组了22/19名TKI治疗后进展的EGFR突变患者,BL-B01D1入组了38名平均治疗线数为3的EGFR突变患者。SKB-264 vs BL-B01D1 vs AK112:ORR(60.0% vs 63.2% vs 68.4%),mDoR(8.7m vs NA vs 8.38m),mPFS(11.5m vs 6.9m vs 8.5m),mOS(22.7m vs NA vs NA)。
针对EGFR野生型NSCLC,BL-B01D1 & AK112响应率良好:SKB-264入组了21名治疗线数≥3的EGFR野生型患者;BL-B01D1入组了50名平均治疗线数为2的EGFR野生型患者;AK-112入组了43名既往未经治疗的晚期无EGFR/ALK基因突变的患者。SKB-264 vs BL-B01D1 vs AK112:ORR(26.3% vs 44.0% vs 53.5%),mDoR(9.6m vs NA vs NA),mPFS(5.3m vs 5.2m vs NA),mOS(14.1m vs NA vs NA)。
整体来看,三个产品的安全性均可控。SKB-264和BL-B01D1均没有出现导致停用的严重TEAEs,未观察到药物相关间质性肺炎的发生,AK-112导致停用的严重TEAEs占比仅2.4%。此外针对≥3级TEAEs,SKB-264和AK-112占比分别达到69.8%、51.8%;针对TEAEs相关死亡事件,AK-112占比达1.2%。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)