2024年慢病新药行业深度分析报告
一、当前市场对信立泰的分歧
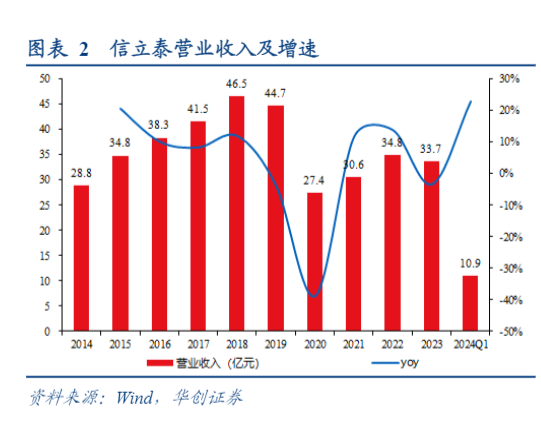
在“4+7”药品带量采购前,依靠泰嘉亮眼的销售表现,信立泰每年都能实现稳定的业绩增长。2019年泰嘉体量突破30亿大关,占据公司制剂收入的近80%,当泰嘉面临集采冲击时,市场担心信立泰未来的增长,股价也应声下跌。经过近两年的调整,公司股价从2018年高点41.98元/股调整至2020年初最低点的15.77元/股。而随着泰嘉集采预期的消化,市场对信立泰的逻辑开始向“集采出清、创新兑现”切换。2020年,一方面信立坦正处在快速放量的阶段,另一方面恩那度司他、JK07、特立帕肽水针、SAL0107几款创新产品先后启动临床,公司创新管线布局逐步清晰,叠加9月公司引入战投凯雷(持股成本33.94元/股),推动信立泰股价快速上涨,2020年市值也基本回到集采前的水平。
但随后2021-2024年至今,我们看到尽管公司几款重磅创新药的研发进度稳步推进,同时早期产品梯队也在不断丰富,但是股价却经历了三年震荡。表观上是市场对信立泰估值的分歧,但背后核心还是对业绩兑现时间节点、兑现程度以及创新产品管线价值的争论,具体则包括以下三个方面:
(一)市场认为公司业绩迟未兑现
在充分消化泰嘉集采丢标影响以及器械子公司计提商誉减值后,市场普遍认为公司后续业绩在低基数下能够维持20-30%的增长中枢。但2022年因医保续约降价以及疫情的扰动,信立坦收入下滑明显;2023年泰嘉天津、福建地区集采续约丢标,对业绩也造成了影响,公司连续两年业绩未能达到市场预期。同时,在创新药保持高强度研发投入的情况下,公司为恩那度司他、SAL0107等已上市以及即将上市的S086等创新药增加销售费用,预计2024-2025年的利润增长仍然处于承压状态,因而市场认为信立泰业绩迟迟难以兑现。
二)对部分创新品种价值的争论
在早期创新药开发上,公司为保证产品成药性以及达到快速上市的目的,选择了fast follow的研发策略。在肾性贫血赛道上,全球首个HIF-PHI药物罗沙司他2018年12月在中国获批,2019年12月信立泰从日本JT公司引进恩那度司他并于2023年6月上市。又如公司立项S086,其与诺欣妥同为ARNI类药物。市场部分观点认为恩那度司他、S086等具有me-too特征,在当前医保控费的背景下,放量难度较大。特别是S086,市场认为在同类ARNI产品诺欣妥即将集采之际,S086作为一款“me-too”产品或难以与一众诺欣妥仿制药竞争。
(三)对公司早期创新管线的忽视
市场对信立泰的关注主要集中在已上市及临床后期的产品,而对早期研发管线关注较少。事实上,信立泰拥有明确的研发职责分工和高效的研发转化效率,集团研究院从AstraZeneca、Pfizer、NIH、Teva等引进高端人才,在深圳、成都、北京和美国等地设立了研发中心和临床医学部门,深圳研究院主要负责小分子创新药研发,美国团队专注于生物大分子的立项开发。通过多年研发投入,公司每年均能保持数款产品IND,实现研发管线的持续扩容,且立项策略从fast follow逐步过渡到first in class,早期管线中不乏JK07、SAL0114、SAL0130等重磅产品。
二、创新管线迎新周期
(一)多款产品进入商业化阶段2023年公司恩那度司他已经上市,2024年5月SAL0107获批,预计2024-2027年公司还将有7款产品获批(未区分适应症),其中复格列汀预计近期获批;2025年公司SAL0108、S086(高血压)、恩那度司他(腹透、血透)、特立帕肽长效也预计将获批,2026年恩那度司他(化疗贫血)、SAL003、SAL0114三款产品有望上市,2027年S086(心衰)和SAL0130预计上市。除复格列汀外,公司其余产品已有较好渠道积淀,公司在心血管领域深耕二十余年,具备强大的客户基础和经验。在竞争激烈的高血压用药市场上,信立坦的成功已证明了公司的创新推广能力,后续上市的新产品也有望借助强大的慢病销售渠道和协同效应实现快速放量。
1、恩那度司他:国内HIF-PHI潜在最优,医保准入后有望快速放量➢罗沙司他年销售额超20亿,奠定HIF-PHI药物在肾性贫血的用药地位2018年12月全球首款HIF-PHI药物—罗沙司他在中国获批,用于治疗慢性肾病引起的贫血。2019年罗沙司他纳入中国医保,价格分别为95.5元/片(50mg)和47.4元/片(20mg),2021年首轮医保续约降价43%,2023年第二次续约降价7%,以此计算罗沙司他目前年费约1.57万元(按每次100mg给药剂量计算)。根据Fibrogen公告,2023年罗沙司他在中国销售收入20.7亿人民币,同比增长36%,2024Q1收入5.8亿人民币,同比增长24%,销量增长39%,即使在较大的收入体量下依然保持较好增长势头。竞争格局方面,根据IQVIA统计中国促红素(EPO)和HIF-PHI两类药物的销售情况来看,2023Q4罗沙司他在肾性贫血用药的销售额占比已经达到42%,成为中国肾性贫血第一大用药。Fibrogen预计罗沙司他治疗化疗引起贫血(CIA)的适应症将于2024年下半年获得NMPA批准,此外,公司还在探索罗沙司他在骨髓增生异常综合征(MDS)的治疗潜力。
恩那度司他为HIF-PHI潜在best in class信立泰的恩那度司他(商品名:恩那罗)已于2023年6月获得NMPA批准用于治疗非透析成人慢性肾病(CKD)患者的贫血治疗,并完成2023年医保准入,4mg规格定价25.93元/片,对应年费9464元。同时公司正在开展恩那度司他透析患者肾性贫血适应症的III期临床,化疗贫血适应症(CIA)也正在临床前准备。从竞争格局来看,国内HIF-PHI竞争格局良好,目前仅罗沙司他和恩那度司他两款上市药物,后续除康哲药业从印度Zydus引进的德度司他已经申报上市(2024年4月)外,其余产品均处在临床早期阶段。
我们认为,恩那度司他并非一款简单的罗沙司他me-too产品,无论是在疗效、安全性还是在依从性方面,恩那度司他都具有明显优势,有望成为国内HIF-PHI类药物最优选择。➢疗效:恩那度司他高选择性抑制PHD1(PHD主要有1/2/3三个亚型,其中PHD1和PHD3型主要作用于HIF-2),更精准稳定HIF-2,因此升高Hb(血红蛋白)水平高效、持久、稳定,经匹配调整间接比较后,恩那度司他Hb达标比例为92.4%,显著优于罗沙司他。同时恩那度司他在降低铁调素的水平上优于罗沙司他,在提升血清铁水平上同样优于罗沙司他。➢安全性:目前的HIF-PHI治疗可能存在作用不精准所导致的Hb升速过快(增加主要心血管不良事件风险)和脱靶方面的风险(过度激活可能引起其他下游靶基因转录,产生贫血以外的脱靶效应如影响脂代谢指标等)。而恩那度司他使用后血红蛋白值稳定、血栓发生率低,生成内源性EPO起效水平低,更贴近生理水平,对脂代谢无影响,潜在脱靶风险小。➢依从性:恩那度司他给药规律、无需体重调节、灵活剂量调整。1)恩那度司他每日给药一次(QD),具有规律性,而罗沙司他每周三次给药(TIW),容易导致患者错服漏服。2)恩那度司他无需根据体重进行调节,而罗沙司他起始剂量需要参照体重进行调节。3)恩那度司他调药次数更少,且主要规格为带刻痕的薄膜衣片,易掰开,调药方式灵活。
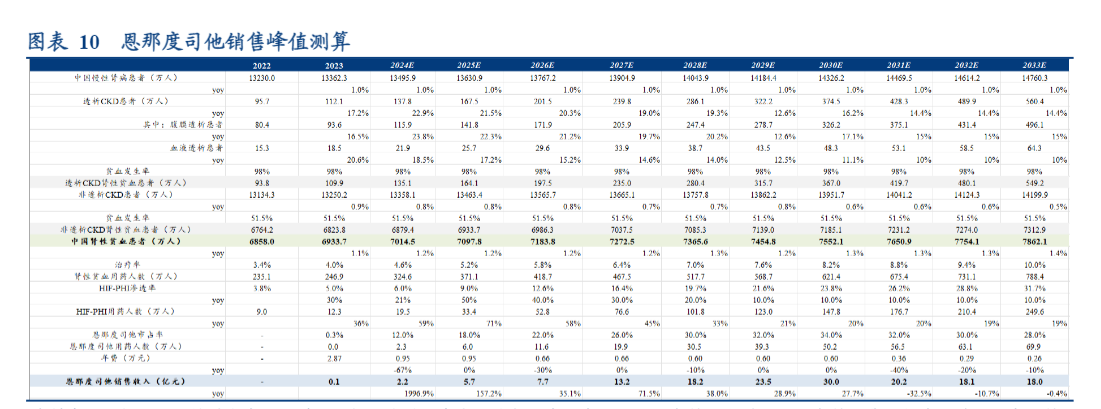
基于信立坦多年肾科推广积累,公司在肾科拥有一定专家和渠道资源,并且2023年公司开始组建肾科专项团队,加大销售资源投入以保障产品放量。目前恩那度司他医院准入态势良好,2024年内即有望为公司带来较好业绩弹性。我们认为,中国肾性贫血市场前景广阔,竞争格局良好,恩那度司他有望成为同类最优,具备成为重磅单品的潜力。根据测算,我们预计恩那度司他销售峰值将达到30.0亿元。
2、S086:诺欣妥集采后,S086或具有更好的放量潜力全球首款ARNI类药物诺欣妥2023年全球销售收入已达到60.4亿美元(+30%),2024Q1收入达18.8亿美元(+34%),在中国市场上,根据中康数据,诺欣妥2023年中国销售额47.6亿人民币(+65%),为高血压和慢性心衰两大慢病领域的重磅单品。
信立泰的S086(沙库巴曲阿利沙坦钙)是全球第二款ANRI药物,S086由沙库巴曲和阿利沙坦酯共晶形成,高血压适应症已于2023年7月向NMPA递交NDA,预计2024年底到2025年初获批;心衰适应症目前正在III期入组阶段,预计2024年底完成入组。诺欣妥核心化合物专利将于2026年11月到期,国内目前获批12款诺欣妥仿制药(但专利期内绝大部分仿制药仍无法销售),市场担心诺欣妥集采后S086的销售会受到压力,但我们认为:第一,从定价逻辑来看,S086高血压适应症预计2025年初获批,参加2025年医保谈判,届时诺欣妥仍处在专利期内,作为国内唯二两款上市的ARNI类药物,S086仍可对标诺欣妥进行定价。因此,我们认为S086并不存在市场所担心的定价压力。
第二,从产业趋势来看,医保改革调整支付结构,提升对创新药的支付空间,同类仿制药被集采后,创新药能够拥有更好的医保支付环境,这个逻辑同样适用于当前医保控费的环境。以信立坦为例,尽管同类沙坦类品种陆续纳入国采,市场规模因大幅降价而萎缩,而信立坦却保持了快速放量态势。又如海思科的环泊酚,2021年上市时丙泊酚中长链也已被集采,从结果来看,环泊酚的放量并没有受到丙泊酚集采的扰动。因此,即使诺欣妥被集采,我们认为S086仍有望依托创新药身份以及过硬的产品力实现放量。
根据测算,我们预计S086的销售峰值将达到47.7亿元,其中高血压适应症峰值20.0亿元,心衰适应症峰值27.7亿元。
在临床上,高血压复方制剂主要用于单药控制效果不佳的高血压患者,并且替代联合给药,提高依从性。信立坦IV期临床研究结果显示,阿利沙坦酯单药控制不佳的临床患者在加用氨氯地平或吲达帕胺后,均能够有效控制血压,有效率均约为60%,为复方产品的研发提供了证据与支持。SAL0107(阿利沙坦氨氯地平)、SAL0108(阿利沙坦吲达帕胺)分别为首个国产ARB/CCB类2类复方制剂和ARB/利尿剂2类复方制剂。SAL0107已于2024年5月获批;SAL0108上市申请已于2023年9月获得受理,有望在2024年底至2025年初获批。两个复方制剂将与已上市的阿利沙坦酯、即将上市的S086高血压适应症形成战略协同,丰富高血压新药管线,满足各类高血压患者用药需求,强化公司在高血压领域的竞争力。
4、特立帕肽:加速市场认知,“老药”焕发新生机骨质疏松用药特立帕肽原研为礼来,2002年美国上市,2011年在中国获批,尽管全球销售峰值达17.5亿美元,但在中国获批的十余年中,由于一直没有做市场教育,导致特立帕肽始终没有放量。根据中康数据,2023年礼来特立帕肽国内收入仅0.3亿人民币。
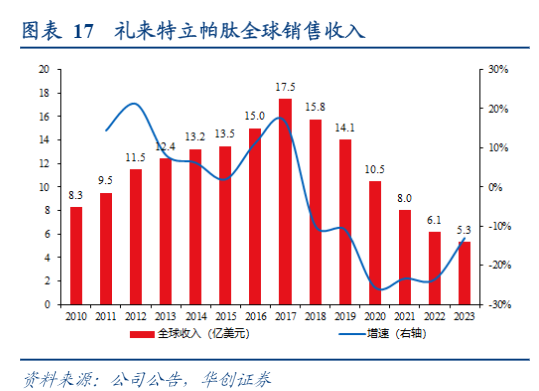
而随着信立泰的特立帕肽上市后,公司正通过市场教育来加快医患认知。信立泰拥有国内最全的特立帕肽产品梯队,2019年特立帕肽粉针获批,水针于2022年4月获得NMPA批准,是首个国产特立帕肽水针,同时,长效剂型上市申请于2024年6月26日获得CDE受理,届时公司将成为国内唯一一家拥有粉针、水针和长效特立帕肽产品的厂商,凭借完善的产品梯队覆盖各类患者需求。根据测算,我们预计信立泰的特立帕肽产品组合销售峰值将达8.0亿元。
5、SAL003:国产PCSK9单抗,有望实现每月给药PCSK9抑制剂是一种全新机制的降血脂药物,相较于现有用药而言,PCSK9抑制剂具有多项优点:可大幅减轻低密度胆固醇(LDL)水平,提供更佳疗效,并为他汀药物不耐受患者提供替代方案;PCSK9抑制剂也有可能降低心脑血管疾病的风险,用于治疗和预防心血管疾病;PCSK9抑制剂具有较低的肝肾毒性风险。目前国内共三款获批上市的PCSK9单抗,安进的依洛尤单抗和赛诺菲的阿利西尤单抗分别于2018年7月和2019年12月获批上市,两款产品2023年合计销售金额接近19亿元,同比增长143%;2023年8月首款国产PCSK9单抗—信达生物的托莱西单抗获批。
信立泰的抗PCSK9单克隆抗体注射液(SAL003)于2019年12月获得临床批准,拟开发适应症为高胆固醇血症和混合型血脂异常,目前正开展“SAL003联合他汀治疗高胆固醇血症和混合型高脂血症的安全性和有效性(CTR20232118)”、“SAL003单药治疗高胆固醇血症和混合型高脂血症的安全性和有效性(CTR20230897)”两项III期临床,预计2024年内完成入组,有望于2025年申报上市。
中国高血脂患者群体广阔,高血脂症群体超一亿,PCSK9抑制剂是一种全新机制的降血脂药物,已展现出较好放量潜力。考虑信立泰在心血管领域丰富的销售经验以及SAL003较强的产品竞争力,我们认为SAL003有望在高血脂这一慢病大适应症上实现快速放量,预计销售峰值达10.4亿元。
(二)早期管线不乏全球first in class品种1、JK07:2024年内II期中期数据展示值得重点关注JK07是美国子公司SalubrisBiotherapeutics自主研发的神经调节蛋白-1(NRG-1)融合抗体药物,拟开发适应症为射血分数减少的慢性心衰(HFrEF)和射血分数保留的慢性心衰(HFpEF),是公司首个中美双报的创新品种,全球尚无同靶点产品。传统抗心衰药物以舒张血管、降低心率、排尿或排钠等间接方法治疗心衰,无法修复心肌细胞结构和逆转心衰过程,因此死亡率一直居高不下。而修复受损的心肌细胞则能从根本上治疗心衰,有望改变当前心衰治疗的现状。
全球首个通过修复心肌细胞结构来治疗心衰的药物为泽生科技的重组人纽兰格林(rhNRG-1)。根据II期试验数据显示,rhNRG-1对心衰患者(NYHA II-III级)效果明显,可在现有心衰标准治疗基础上进一步明显提高患者左室射血分数(绝对值提高3%-5%),降低心脏收缩末期容积,修复心脏细胞。但是rhNRG-1在临床应用中存在三大关键限制:由于NRG-1激活了HER3通路而导致:1)患癌风险增加、2)潜在胃肠道毒性、3)NRG-1半衰期过短(泽生科技rhNRG-1临床试验中需连续10天每日静滴10小时,患者依从性差)。相比于rhNRG-1,JK07融合了NRG-1片段和抗HER3抗体两个蛋白片段,既降低了患癌风险和胃肠道毒性,同时也解决了NRG-1半衰期短的问题。通过独特的分子设计,解决了rhNRG-1蛋白疗法的局限性,提高成药性和安全性。
根据JK07披露的Ib数据显示,JK07美国Ib临床共纳入14名NYHA II/III级心衰患者,研究包括三个剂量组(0.03mg/kg、0.09mg/kg和0.27mg/kg)。试验结果显示,JK07单次给药6个月内可使LVEF呈现具有临床意义的改善,0.09mg/kg剂量组患者180天后LVEF平均改善达49%,LVEF重回40%水平。安全性方面,JK07总体耐受性良好,大多数不良事件为轻度至中度,仅在0.27mg/kg组发生一例严重不良事件(3级)。
目前,JK07已经启动关于HFrEF、HFpEF两个适应症的II期国际多中心,美国、中国、加拿大三个国家合计目标入组282人,区分为JK07低剂量组和高剂量组。结合I期疗效、安全性以及样本量数据来看,我们推断JK07或将先通过低剂量组(0.03mg/kg-0.09mg/kg区间内的剂量水平)进一步确认大样本量情况下的安全性数据,然后再通过高剂量组(大概率为0.09mg/kg)来确认疗效。根据ClinicalTrials显示,JK07目前已正式启动患者入组,预计2024年底前读出部分低剂量患者的中期数据。除心衰领域外,JK07也在开发神经治疗领域的应用。NRG-1作为一种神经调节蛋白,可促进神经系统发育,抑制神经元凋亡,诱导细胞因子的表达,如果NRG-1或NRG1/ERBB发生异常,可能造成如肌萎缩性侧索硬化症(ALS)、阿尔茨海默症(AD)等神经系统相关疾病,目前JK07关于ALS适应症正处于临床前研究阶段。
2、SAL0130:全球首款ANRI+CCB复方,补全高血压用药拼图既往高血压防治指南推荐的常用降压药物包括CCB、ACEI、ARB、利尿剂和β受体阻滞剂五类及由上述药物组成的单片复方制剂(SPC),2023新版高血压防治指南补充了ARNI作为新一类常用降压药物,以上六类降压药物和SPC均可作为初始和维持治疗的常用药物,并且将CCB+ARNI、ARNI+利尿剂新增推荐为优化联合治疗方案。在“药物联用”和“单片复方制剂”方面,指南认为单片复方制剂使用方便,可改善治疗的依从性及疗效,正成为联合治疗的新趋势。在亚洲人群进行的一项多中心、双盲、随机对照研究证实,对于CCB治疗后不达标的高血压患者,ARNI+CCB联合治疗比CCB单药进一步降低24小时动态血压SBP(收缩压)13.1mmHg和DBP(舒张压)7.7mmHg。高血压防治指南的推荐以及真实世界循证支持,均提示ARNI+CCB复方制剂具备较好市场潜力。基于此,公司设计SAL0130(S086+氨氯地平复方),为全球首个ARNI+CCB的复方。产品立项以来,SAL0130临床快速推进,由于S086在国内尚未获批上市,目前公司先开展S086、苯磺酸氨氯地平联合给药的III期临床。待S086在中国获批后,补充“SAL0130复方头对头S086单药的III期临床”、“SAL0130复方与S086、氨氯地平联合用药生物等效性试验”后即可申报上市,有望于2027年获批。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)