2024年科伦博泰生物ADC药物市场分析报告
1.国内ADC领军创新药企
1.1 依托科伦雄厚资源,打造领域旗舰
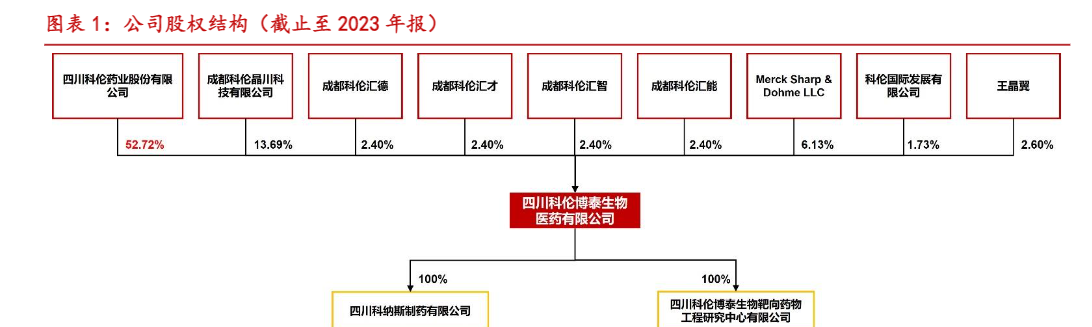
四川科伦博泰生物是一家专注于创新药物研发、制造及商业化的生物医药公司,自2016年成立以来,始终致力于解决中国乃至全球的医疗需求。凭借一体化的药物开发能力及涵盖所有关键业务功能的完善的管理机制,科伦博泰致力于内部开发差异化的治疗方法,以支持提高现有的医疗健康水平。作为抗体药物偶联物(ADC)先驱及领先开发者之一,科伦博泰在ADC开发方面积累了超过十年的经验,是中国首批也是全球为数不多的建立一体化ADC研发平台OptiDC 的生物制药公司之一。公司股权结构稳定,默沙东成为第二大股东。根据企业2023年年报,四川科伦药业持股52.72%,四个员工激励平台(科伦汇德、科伦汇才、科伦汇智、科伦汇能)合计持股9.60%,默沙东与公司深度合作,持股6.13%。公司控股子公司共有两家,分别为四川科纳斯制药有限公司和四川科伦博泰生物靶向药物工程研究中心有限公司。
管理层稳中有新,高管团队呈现新老搭配格局,赋能科伦博泰创新动力。科伦药业创始人兼董事长刘革新任公司董事长,科伦药业老将葛均友任公司总经理。科伦博泰创立之初,便布局ADC药物研发,为后续管线扩张提供强大内生动力。而后又积极引进跨国药企人才,包括谭向阳、金小平、郭永等人,从药物创新研发到商业化销售全方位助力公司发展。
1.2 优势ADC技术平台助力创新研发
公司已搭建“OptiDC”平台(抗体偶联药物平台),是抗体偶联药物(ADC)的先行者及领先开发商之一。经过十多年的发展,已开发出一套ADC核心组件库,能够设计出针对不同生物靶点进行优化的定制ADC,以解决各种适应症中的医疗需求。截至2023年6月20日,该平台已通过临床前研究及临床试验对超过1200名患者进行测试及验证。已经通过广泛的研究和试验,包括十多项临床或临床前候选药物的验证。在SKB264等项目中完美地展现了公司ADC Kthiol策略的设计与优化主要技术,包括不可逆的抗体偶联技术、pH敏感型连接子、中等活性的细胞毒素以及高载荷(DAR7.4)的定点定量策略等。➢抗体:自主研发新型抗体,具有高抗原亲和力和高特异性。➢不可逆的抗体偶联技术&pH敏感型连接子:利用公司专有的Kthiol药物连接子策略,改善了ADC的稳定性,以及减少脱靶及在靶脱瘤毒性。与Trodelvy中马来酰亚胺与半胱氨酸的可逆连接不同,SKB264的连接子通过与二硫化物还原的半胱氨酸的不可逆共价结合,与作为适配体的甲磺酰基嘧啶偶合。这可以防止有效载荷在循环中轻易从ADC上脱落。一旦到达肿瘤部位,连接子中的碳酸盐切割部分便可以令有效载荷快速释放以发挥杀伤作用。这种创新设计增强SKB264的靶向能力,减少其脱靶及在靶肿瘤外毒性,因此有潜质实现更广泛的治疗窗口。➢中等活性的细胞毒素&高载荷:在另一项使用相同CDX模型与Trodelvy进行的头对头研究中,在研究中测试的所有三种剂量(1、3、10mg/kg)中,与剂量相同的Trodelvy相比,使用SKB264治疗的TGI第21天优于Trodelvy的TGI。这表明SKB264可以以较低的剂量给药以最大限度地减少不良反应,同时保证相当甚至更好的疗效。
此外,公司已建立四位一体平台体系,包括:新药研究平台、临床研发平台、生产及质量平台、商业化销售平台,具有从创新药物开发到商业化销售的全流程战略能力,能够快速推进管线进展。
1.3 联手默沙东,进军全球市场
科伦博泰的管线价值与药物平台开发能力得到了全球战略合作伙伴的认可。与默沙东深度合作,在2023年1月的B轮融资中,默沙东向科伦博泰注资1亿美元,现持有了科伦博泰6.13%的股份。同时默沙东在项目上引进科伦博泰多项ADC候选药物项目的开发权益,2022年科伦博泰与默沙东先后达成3笔BD交易,交易合计总金额已经超过118亿美元。默沙东K药的关键专利将在2028年到期。科伦博泰的OptiDC平台为默沙东K药赋能,以期寻找联合用药疗法延长K药生命周期,对于K药的合作成为了科伦博泰进军全球市场的重要机遇。
2.ADC管线布局全面
凭借多技术平台的核心创造力,公司目前拥有众多临床价值高的产品管线,整体呈现以ADC药物为核心,大分子/小分子药物并行的格局。
2.1 SKB264:全球第一梯队,海外进展顺利
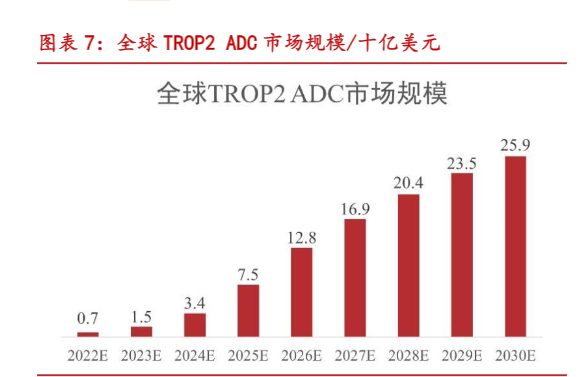
人滋养层细胞表面抗原2(Trop2)是一种细胞表面糖蛋白,可传导细胞内钙信号和细胞外信号通路,在肿瘤细胞增殖、凋亡和侵袭中起重要作用。它在多种肿瘤中过度表达,例如胰腺癌,卵巢癌,前列腺癌和乳腺癌等,是一个泛癌靶点,市场前景广阔。根据弗若斯特沙利文预测,全球TROP2 ADC市场规模预计将由2022年的7亿美元增长到2030年前的259亿美元,年复合增长率为57.0%。中国TROP2 ADC市场预计由2023年的2亿元增长到2030年前的236亿元,年复合增长率为97.7%。
目前TROP2 ADC全球仅吉利德公司Trodelvy获批,2023年全球收入10.63亿美元。在美国获批了三个适应症:晚期TNBC(3L+)、晚期UC(2L)以及HR+/HER2-BC(3L+);在中国,于2022年6月获批上市,用于治疗不可切除晚期转移性TNBC(3L+)。
对于TROP2 ADC靶点的研发而言,目前国内研发进度在III期及以上的项目共五个:吉利德公司的Trodelvy已获批、科伦博泰的SKB264及第一三共的DS-1062处于NDA阶段,三款药物进展相对领先。
SKB264是公司的核心ADC产品,具有以下特性:高DAR值(7.4);高抗原亲和力及靶向效应;全新的碳酸盐连接子,利用肿瘤的酸性微环境选择性释放细胞毒性载荷;使用新型拓扑异构酶I抑制剂,具有中等的细胞毒性。相较于其他TROP2 ADC,SKB264差异化的分子设计富有竞争力。
在非头对头针对三阴乳腺癌适应症的临床数据比较中,疗效数据和安全性数据都显著优于Trodelvy,同时还优于第一三共的DS1062,展现出了同类最佳的潜质
在海外市场,迄今为止,为探索与科伦博泰合作开发的MK-2870的应用潜力,默沙东已启动了8项注册性临床试验以评估其在不同类型肿瘤中的治疗效果,药物出海抢占市场未来可期。
2.2 A166:HER2 ADC,商业化在即
A166是公司目前已处于NDA申报阶段的HER2 ADC,,采取高载荷低毒性DAR设计,通过稳定酶可裂解连接子将新型高细胞毒性微管蛋白抑制剂duostatin-5在低DAR的条件下与具有与赫赛汀(曲妥珠单抗)相同的氨基酸序列的HER2单抗进行定点偶联。A166已达到其针对晚期HER2+ BC的关键性II期试验的主要终点,并于2023年5月提交NDA申请。
2.3 CLDN18.2:消化道领域新晋热门靶点
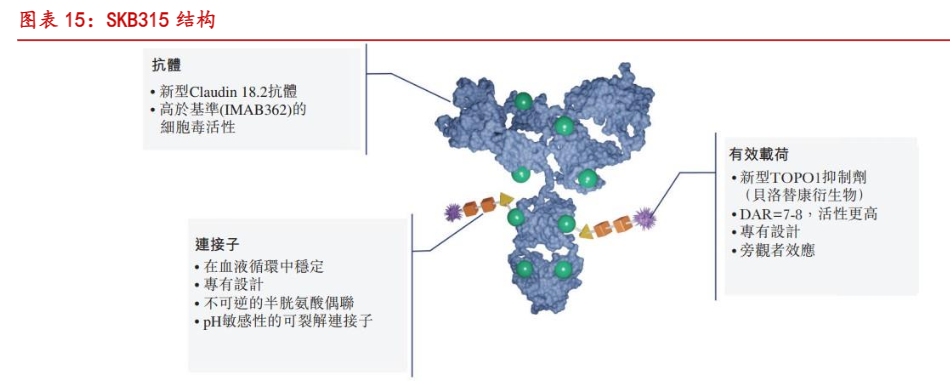
CLDN18.2是一种细胞连接蛋白,表达严格限于胃黏膜或胃壁的最内层,在正常情况下,很大程度上无法与靶向抗体接触。然而,在癌症发展过程中,细胞连接被破坏,使肿瘤细胞表面的CLDN18.2表位暴露出来,成为特定的靶点。除胃癌外,CLDN18.2被发现在其通常不表达的各类器官肿瘤(例如胰腺癌及食道癌)中过度表达,使其成为开发靶向疗法的潜在候选靶点。公司开发的SKB315具有专有、内部开发的人源化CLDN18.2单抗,连接子采用的是pH敏感的可裂解连接子,采用高DAR搭配中等毒性毒素的设计。
目前国内关于CLDN18.2 ADC管线进入临床核心攻坚期,进入III期临床的包括信达生物的IBI343、康诺亚的CMG901、礼新医药的LM-302及恒瑞医药的SHR-A1904。目前国内关于CLDN18.2 ADC管线进入临床核心攻坚期,进入III期临床的包括信达生物的IBI343、康诺亚的CMG901、礼新医药的LM-302及恒瑞医药的SHR-A1904。
2.4Nectin-4:尿路上皮癌
Nectin-4(PVRL4)作为Nectin家族的跨膜多肽,在许多实体瘤中表达,是一种包括尿路上皮癌在内的多种实体中高度表达的治疗靶点。经发现,Nectin-4在尿路上皮癌患者的93%样品中高度表达。针对Nectin-4开发的ADC疗法处于初步阶段,临床疗效及药物连用或成突围关键。Nectin-4(PVRL4)作为Nectin家族的跨膜多肽,在许多实体瘤中表达,是一种包括尿路上皮癌在内的多种实体中高度表达的治疗靶点。经发现,Nectin-4在尿路上皮癌患者的93%样品中高度表达。针对Nectin-4开发的ADC疗法处于初步阶段,临床疗效及药物连用或成突围关键。
3.非ADC产品即将进入兑现期
目前公司在研的非ADC产品包括单/双抗药物和小分子药物,布局疾病包括肿瘤和非肿瘤领域,同时具有短期收获现金流和未来发展的潜力。目前公司在研的非ADC产品包括单/双抗药物和小分子药物,布局疾病包括肿瘤和非肿瘤领域,同时具有短期收获现金流和未来发展的潜力。
3.1A400:高选择性RET抑制剂,有望克服耐药
A400是新一代高选择性RET抑制剂,对RET的抑制作用远高于VEGFR、JAK1和JAK2。A400采用新型专利分子结构设计,解决选择性RET抑制剂耐药性,同时保持靶点选择性、疗效和安全性并能够降低生产成本和难度。临床前研究证明A400对多种RET变异及CNS渗透有强效。目前国内已有两款进口获批上市,首药控股的SY-5007位于III期临床,科伦博泰A400 已经进入II/III期临床,进度位于前列,有望实现研发突围。
3.2A223:进军自身免疫病,市场未来可期A223为选择性抑制JAK1及JAK2两种主要类型JAK的小分子。JAK-信号转导及转录激活物通路是细胞因子转导细胞外信号以诱导炎症、控制免疫应答及协调造血功能的关键信号途径。JAK是一组与细胞因子受体相关的四种酶,在细胞因子暴露后会被激活。通过其酶活性,被激活的JAK吸收及激活下游信号分子STAT,驱动细胞核中的细胞因子应答基因表达程序。目前共有6款JAK抑制剂在国内获批上市,分别为乌帕替尼、巴瑞替尼、托法替布、芦可替尼、阿布昔替尼、利特昔替尼,适应症覆盖类风湿性关节炎、克罗恩病、斑秃、特异性皮炎等多种自身免疫性疾病。
3.3A167:联用治疗新机遇科伦博泰开发的泰特利单抗注射液(产品代号:KL-A167注射液)提交的上市许可申请获得国家药监局药品审评中心注册受理。目前国内尚无具有自主知识产权的国产PD-L1单抗获批,KL-A167注射液是全球首个拥有自主知识产权的用于治疗既往接受过二线及以上化疗失败的复发或转移性鼻咽癌的PD-L1单抗。
3.4A140:西妥昔单抗生物类似药获批在即根据弗若斯特沙利文统计及预测,中国EGFR单抗市场由2017年的人民币8亿元增至2022年的人民币41亿元,复合年增长率为37.3%,根据弗若斯特沙利文预测中国EGFR单抗市场预计将于2030年达到人民币106亿元。目前国内西妥昔单抗及其类似药,原研已获批,公司A140进度靠前处于NDA阶段。
4.盈利预测与估值
盈利预测考虑公司临床后期核心管线(3期及以上)的国内销售额,以及SKB264海外权益部分(包括销售分成及里程碑),海外里程碑部分考虑未来1-3年内默沙东有望启动Trop2/CLDN18.2/Nectin4等ADC进入注册临床阶段,因此假设2024-2026年公司每年收到约1亿美金里程碑。国内方面,我们预计公司2025年有五款商业化产品:包括SKB264(Trop2 ADC,2023年12月NDA受理)、A166(HER2 ADC,2023年5月NDA受理)、A167(PD-L1,2021年11月NDA受理)、A140(西妥昔单抗生物类似药,2023年9月NDA受理)、A400(RET抑制剂,预计今年提交NDA)。我们预计公司2024-2026年总营收分别为8.03/13.06/22.81亿元。
采用DCF估值方法,通过Wind BETA计算器参考行业beta计算得公司调整后beta为1.1,无风险收益率假设为十年期国债收益率(2.24%),市场预期收益率假设为8%,有效税率假设为15%,债务资本成本Kd假设为4.20%,债务资本比重Wd假设为3.25%,股权资本成本Ke假设为8.58%,经计算得出加权平均资本成本WACC为8.41%;费用情况:根据公司2023年报披露,由于进入临床后期管线增多,研发费用有所升高,并且公司即将进入商业化阶段,因此我们假设未来三年研发费用基本持平,后期研发费用率稳定在18%;未来三年销售与管理费用有大幅增加,后期销售与管理费用率稳定在21%。公司拥有丰富的产品管线和较强的自主研发能力,核心管线打开国际市场。通过DCF方法计算,假设永续增长率为2%,WACC为8.41%,公司合理股权价值为472亿元,对应510亿港元(汇率取人民币1元=1.08港元)。首次覆盖,给予公司“买入”评级。
国际化平台创新药企,打造ADC领域旗舰地位。四川科伦博泰生物是科伦药业控股子公司,成立于2016年,2023年7月在港交所正式上市,并于2024年3月纳入港股通成分。公司专注于生物技术药物及创新小分子药物的研发、生产、商业化及国际合作。通过优势研发平台打造丰富且全面的ADC创新管线,并与国际巨头药企达成战略合作,进军国际市场。➢“OptiDC”研发平台助力公司ADC管线持续扩容,默沙东积极推进国际化进展。目前公司呈现以ADC药物为核心,单抗、双抗、创新靶点小分子药物等热点领域并进的研发格局。目前公司已有4款的ADC药物进入临床阶段,覆盖ADC核心靶点TROP2,HER2,CLDN18.2,Nectin-4。此外,公司还有多款的临床前ADC药物储备。公司与默沙东的深度合作使得科伦博泰成为默沙东ADC管线最重要的合作伙伴,核心管线在国际市场未来空间广阔。➢SKB264(Trop2 ADC)国内获批在即,海外临床加速推进:国内方面,3L TNBC已于2023年12月NDA获受理,有望今年获批;EGFRmt TKI耐药NSCLC有望今年提交上市申请;1L TNBC和2L+ HR+/HER2-BC 处于注册临床阶段;1L HR+/HER2-BC(ET失效后)和1L EGFRwt NSCLC有望今年进入注册临床。海外方面,默沙东自2023年10月份以来,已密集启动8项全球三期临床,作为临床突破的重要切入点之一,旨在覆盖更广阔的癌种和积极向前线拓展。K药+SKB264的强强联手有望延续默沙东K药生命周期,挖掘广阔市场。
5.风险提示
临床研发失败风险:创新药研发具有较大不确定性,II期到III期阶段因为疗效不及预期而失败的比例较高,III期由于受试者的数量增多,以及临床试验过程中的影响因素增多,可能导致临床数据不及II期而研发失败。竞争格局恶化风险:公司核心布局产品虽然进度较为领先,但临床上已有竞争对手布局,存在未来竞争格局恶化风险。销售不及预期风险:产品销售受到本身特性,竞争格局,销售队伍,行业发展等多方面因素影响。行业政策风险:进入医保的创新药品种增多加之近几年疫情的支出影响,医保基金的压力逐年增加,可能导致药物的谈判价格不及预期,存在受到行业政策或监管政策影响的风险。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)