2024创新药行业报告:产品销售增长,费用控制优化
创新新药药板板块块::营营收收加加速速增增长长,,费费用用率率、、利利润润率率水水平平改改善善
创新药子行业2023全年营收总额同比+16.7%,2024Q1营收总额同比+30.8%。除了新上市/新进入医保的产品的销售放量之外,部分公司对外授权的收入也为整体的营收带来较大的增量。同时,行业整体的归母净亏损大幅收窄,主要是因为在营收大幅增长的同时,各项费用率均有一定的下降。
2023全年创新药子行业的毛利率为79.7%(+1.6pct),销售费用率33.3%(-5.4pct),管理费用率12.6%(-2.1pct),研发费用率38.6%(-6.1pct);2024年Q1创新药子行业的毛利率为84.3%(+0.2pct),销售费用率34.7%(-2.1pct),管理费用率14.4%(-2.2pct),研发费用率43.5%(-8.1pct)。公司通过合理的费用控制和投入,23年各项费用与去年同期基本持平,而费用率同比有较大幅度的改善。n创新药核心单品及更多的产品组合使创新药整体销售收入仍呈向上突破趋势。
我们认为,随着集采对存量仿制药业务的影响逐步消退,创新药进入医保后快速放量,行业中长期的、创新驱动的成长将会逐步兑现。另一方面,随着费用率水平的改善,一些优秀的biotech公司有望在未来的1~2年内实现盈利,通过自身的造血能力去支持后续管线的开发。
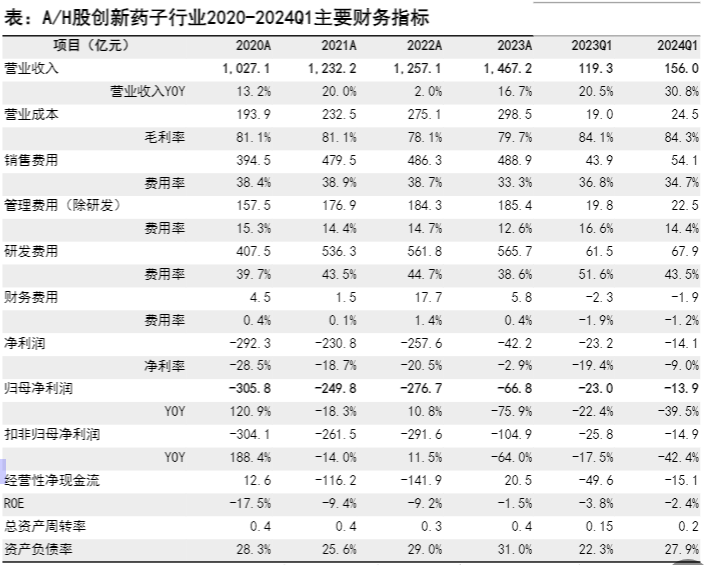
营收收增增长长强强劲劲,,产产品品销销售售驱驱动动力力强强
营收增长强劲,大部分为产品销售驱动。我们选取了16家已经实现商业化、并具备一定销售体量的biotech公司作为样本,对于biotech公司2023年的财务情况进行分析。从营收端看,剔除授权合作等收入后,全部16家公司的产品销售均实现正增长。除了康方生物、和黄医药的营收中包含大额的合作收入的影响之外,大部分公司的营收增长主要由产品销售驱动。其中,产品销售增速在100%以上的公司有2家,增速在50%~100%的公司有4家,增速在30%~50%的公司有4家,增速在10%~30%的公司有5家,增速在10%以下的公司有1家。
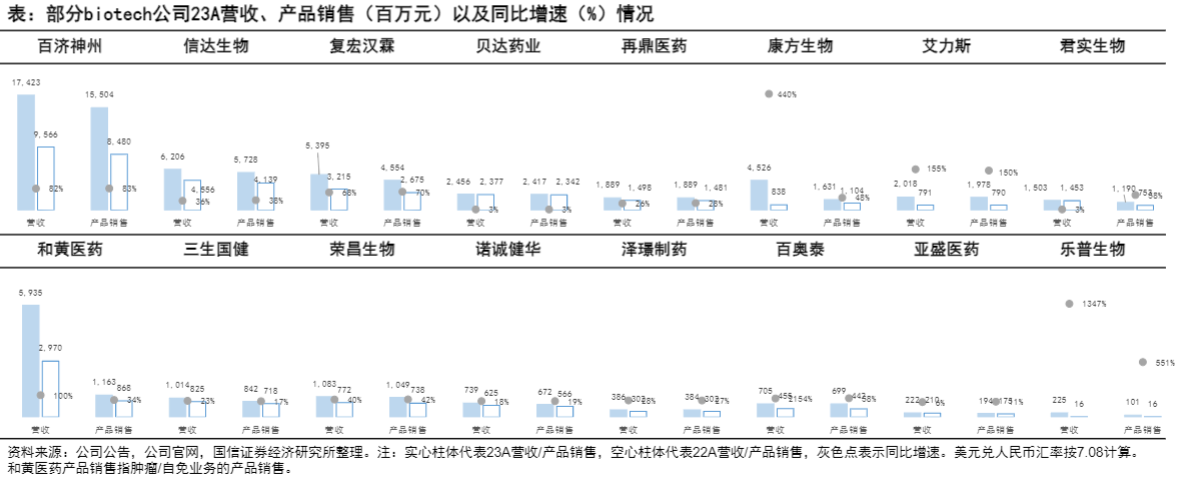
销售费用率显著下降。在上述样本biotech公司中,除诺诚健华2023年销售费用同比下降(-16%)外,其余公司的销售费用均有所增加;但随着销售规模的扩大,部分公司的销售费用率(以销售费用/产品销售计算)出现明显的下降。其中,销售费用率同比下降10~30pct的公司有4家,同比下降0~10pct的公司有5家,同比上升0~10pct的公司有4家,同比上升10pct以上的公司有3家。随着biotech公司销售规模不断扩大,销售团队趋于稳定,我们预计公司的销售费用率在未来会有持续的下降。
研发发费费用用的的投投入入更更加加聚聚焦
研发费用的投入趋于谨慎、合理。在当前的大背景下,biotech公司对于研发费用的投入也变得更为谨慎,且更加聚焦在核心的、后期的管线:2023年仅有5家公司的研发费用增长超过10%(诺诚健华、艾力斯、荣昌生物、百济神州、百奥泰),仅有1家公司的研发费用增速在0~10%之间(泽璟制药),另外10家公司的研发费用则出现了小幅下降。
越来越多的公司实现商业化盈利。由于大部分biotech公司仍处于亏损状态,我们简单还原研发费用之后,对比公司的商业化盈利能力(即药品销售收入-成本-销售费用-管理费用)。可以看到,23全年实现商业化盈利的公司达到了10家(去年同期为7家);并且,仅有2家公司的商业化盈利是下滑的。同时,各家公司的商业化盈利(亏损)/产品销售的比值普遍升高。另外,实现商业化销售较早的贝达药业、三生国健,研发投入合理且销售快速增长的艾力斯、复宏汉霖等公司已经实现了报表端的盈利。
头部部BBiiootteecchh公公司司的的现现金金储储备备良良好好
基于当前的发展阶段,绝大部分Biotech公司产品销售产生的现金流不足以支撑每年的研发、生产等的支出,我们简单对比了公司的在手现金(包括银行存款以及其他短期投资)以及经营性支出(产品销售-销售费用-管理费用-研发费用)的情况。头部Biotech公司的现金储备良好,与经营性支出的比例大部分在200%以上,足以支持公司的正常经营,以待核心产品的销售放量。
恒瑞瑞医医药药::2233年年创创新新药药实实现现较较快快增增长长,,创创新新药药占占比比持持续续提提升
2023年财务数据:恒瑞医药2023年实现营收228.20亿元(+7.26%),归母净利润43.02亿元(+10.14%),扣非归母净利润41.41亿元(+21.46%),经营性现金流净额76.44亿元(+504.12%),其中创新药收入(含税,不含对外许可收入)106.37亿元(+22.10%)。公司2023年度,累计研发投入61.50亿元,其中费用化研发投入49.54亿元(+1.38%),销售费用为75.77亿元(+3.12%),管理费用为24.17亿元(+4.79%)。
多款新药产品上市销售,数个适应症拓展获批。2023年公司共有7款新药获批上市,3款1类创新药(阿得贝利单抗、磷酸瑞格列汀、奥特康唑)、4款2类新药(盐酸右美托咪定鼻喷雾剂、醋酸阿比特龙纳米晶、盐酸伊立替康脂质体、恒格列净二甲双胍缓释片)。
临床试验稳步推进,管线储备丰富。2023年全年,共有14项产品上市申请获得受理,12条管线推进至临床III期,35条管线进展到临床II期,30条管线进展至临床I期;72个创新药临床获批,5项获得突破疗法认定。
国际市场中获得认可,多款产品实现出海。在2023年ASCO会议中,8款抗肿瘤创新药的57项研究成果入选,其中2项为大会口头报告;13款抗肿瘤创新药的35项研究结果入选2023年ESMO大会,其中7项入选大会口头报告。
2023年,5款产品实现海外授权,交易总额超过40亿美元。2024年5月,公司GLP-1组合产品有偿授权给美国Hercules公司,并且获得Hercules公司19.9%股权、最高超60亿美元的相关付款和销售分成。
海思思科科::麻麻醉醉产产品品销销售售收收入入同同比比增增长长9944..55%%,,创创新新管管线线进进入入收收获获期
麻醉产品销售收入快速增长,环泊酚有望年内在美国提交NDA。2023年,公司实现营收33.55亿元(同比+11.3%),归母净利润2.95亿元(同比+6.5%),扣非归母净利润2.42亿元(同比+153.2%)。2024Q1,公司实现营收7.52亿元(同比+20.6%),归母净利润0.92亿元(同比+219.9%),,扣非归母净利润0.3亿元(同比+4.4%)。分产品看,麻醉产品实现销售收入8.50亿元(同比+94.5%),核心产品环泊酚目前在国内已获批“非气管插管手术/操作中的镇静和麻醉”、“全身麻醉诱导和维持”、“重症监护期间的镇静”等适应症,“全麻诱导”适应症的美国Ph3临床研究顺利推进中,年内有望提交NDA申请;肠外营养系产品实现销售收入6.15亿元(同比-4.1%),毛利率60.79%(同比-4.9pp);肿瘤止吐和肝胆消化产品分别实现销售收入2.12/0.67亿元,分别同比-20.3%/+1.5%,核心产品思复(多烯磷脂酰胆碱注射液)和立必复(甲磺酸多拉司琼注射液)于2023年完成销售模式转换,全面回收医院终端转为自营团队专业化学术推广模式。
12n创新药转型初见成效,临床管线进入收获期。目前,公司有12个进入临床阶段的1类创新药管线。其中,HSK16149(思美宁)“糖尿病外周神经痛”适应症有望在2024年获批上市,“带状疱疹后神经痛”适应症上市许可审评中;镇痛药物HSK21542注射剂型“腹部手术术后镇痛”适应症已于2023年10月申报NDA,目前在审评中;超长效降糖药物HSK7653片于2023年12月完成了发补研究并递交相关资料,目前在发补审评中。
核心产品派格宾销售同比增长54%。2023年公司实现营收21.00亿元(同比+37.6%),归母净利润5.55亿元(同比+93.5%),扣非净利润5.79亿元(同比+73.6%)。分产品看,核心产品派格宾实现销售17.90亿元(同比+54.2%),占营收比例达到~85%,是公司业绩增长的主要驱动力,毛利率95.52%(同比+6.0pp),主要由于减少了专利使用费支出,派格宾毛利率大幅改善;特尔津、特尔康、特尔立分别实现营收1.60/0.87/0.46亿元(分别同比-16.2%/-12.0%/-31.4%),销售量分别为916.57/183.99/153.47万支(分别同比+4.7%+4.7%/-26.5%);珮金(YPEG-G-CSF)于2023年6月30日获批上市,2024年作为首个完整销售年,有望贡献销售增量。n核心品种派格宾目前是国内市场唯一的长效干扰素产品。
派格宾是全球首个40kD聚乙二醇干扰素α-2b注射液,于2016年在国内获批上市。基于抑制病毒复制和增强免疫的双重作用,派格宾获批适应症为慢性乙型/丙型肝炎(180μg剂量qWx48);2024年3月,新增联合核苷(酸)类似物适用于临床治愈成人慢性乙型肝炎适应症申请获受理。国内共有3款长效干扰素产品获批上市,其中Merck/先灵葆雅的佩乐能(2016年2月起停产)、Roche的派罗欣(国内合作方歌礼制药于2022年底停止提供推广服务,Roche将不再寻求其他合作方,也不会在国内继续开展派罗欣的商业推广)已退出中国市场,短期内公司派格宾为国内市场唯一长效干扰素产品。
智翔翔金金泰泰::在在研研管管线线有有序序推推进进,,赛赛立立奇奇单单抗抗获获批批在在即即
加大研发投入,在研管线有序推进。2023年,公司实现归母净利润-8.01亿元,亏损有所扩大,主要系公司多款新药产品处于在研状态,各项新药研发项目有序推进,研发投入较上年同期增加。其中,2023年研发支出合计达6.20亿元(同比+36.5%)。公司现有在研管线15个,其中9个产品17个适应症获批进入临床,2个适应症NDA已获受理,2个适应症处于Ph3临床阶段,覆盖自身免疫性疾病、感染性疾病、肿瘤等治疗领域。
核心品种GR1501/赛立奇单抗获批在即,国内进度领先。GR1501是国内首个申报上市的国产抗IL-17A单抗,中重度斑块状银屑病适应症Ph3临床数据优异,第52周达到PASI75及PASI90的受试者比例分别为96.5%/84.1%、达到PGA(0~1)的受试者比例为84.4%,疗效显著且持久。
公司公告,国信证券经济研究所整理nGR1802中重度特应性皮炎适应症Ph3临床完成首例受试者入组。公司IL-4Rα抗体GR1802于2024年初完成中重度特应性皮炎适应症Ph3临床首例受试者入组;慢性鼻窦炎伴鼻息肉、慢性自发性荨麻疹、哮喘、过敏性鼻炎等适应症处于Ph2临床试验阶段,整体进度紧跟国内第一梯队。
迈威威生生物物::NNeeccttiinn--44AADDCC多多适适应应症症快快速速推推进进临临床
2023年财务数据:迈威生物2023年实现营收1.28亿元(+361%),营收大幅增长主要是因为公司的9MW3011项目对外授权并收到首付款1000万美元,同时实现药品销售收入0.42亿元;公司全年净亏损10.53亿元(上年同期亏损9.55亿元)。公司2023年度研发费用为8.36亿元(+10.2%),销售费用为1.43亿元(+82.0%),管理费用为2.25亿元(+19.2%)。
核心产品商业化推进良好。公司2023 年实现了两款产品的商业化:阿达木单抗(君迈康)和地舒单抗(迈利舒)。其中,君迈康完成发货约16.7万支,完成26省招标挂网,准入医院173家,覆盖药店1316家;迈利舒完成发货约8.4万支,完成28省招标挂网,准入医院605家,覆盖药店2061家。
Nectin-4ADC多适应症快速推进临床公司的核心产品9MW2821(Nectin-4ADC)已在2023年底开启3L UC适应症的3期临床,研发进度全球第二,且在国产同靶点产品中领先优势较大;在RP2D下,9MW2821在末线UC的ORR=62.2%,DCR=91.9%,mPFS=6.7mo,具备BIC潜力。另外,9MW2821单药在后线宫颈癌和食管癌中也取得了优秀的早期临床数据,预计将进行3期临床的推进。另一方面,9MW2821 联合PD1单抗在一线治疗中的应用也在进行早期的临床探索。
君实实生生物物::披披露露22002233年年业业绩绩和和管管线线进进展展
2023年财务数据:君实生物2023年实现营业收入15.03亿元,同比增长3.38%;其中拓益销售收入为9.19亿元,同比增长24.93%;销售费用8.44亿元(+17.98%),研发费用19.37亿元(-18.74%),管理费用5.36亿元(-5.74%);归母净利润-22.83亿元,亏损同比减少1.05亿元。
核心管线进展:2023年核心产品拓益(特瑞普利单抗)在国内有7个适应症获批,其中6个适应症进入医保,3个新增适应症上市申请获得受理;23年10月在晚期鼻咽癌适应症获得FDA批准,并于今年1月正式在美国市场销售,成为首个FDA批准上市中国自研和生产的创新生物药,也是美国首个且唯一一款治疗鼻咽癌的药物,同时被NCCN指南首选为一类推荐。民得维获NMPA附条件批准上市,并纳入医保目录。君迈康8项适应症获NMPA批准,并全部纳入国家医保目。
Tifcemalimab(BTLA)针对LS-SCLC适应症的国际多中心III 期临床已经完成全球FPI及首次给药;针对cHL适应症在中国启动III期临床研究。昂戈瑞西单抗(PCSK9)2项适应症上市申请获NMPA受理;JS005(IL-17A)针对中重度斑块银屑病适应症进入III 期注册临床研究。n2024年里程碑事件:2024年公司的特瑞普利单抗预计拓展TNBC、肾癌(1L)、SCLC(1L)适应症,积极开拓海外市场,多项临床数据预期读出并申报上市,同时BTLA、IL-17A、PI3K-α、PD-1等靶点药物可能推进到关键临床。
三生生国国健健::披披露露22002233年年业业绩绩和和管管线线进进展
2023年财务数据:三生国健2023年实现营业收入10.1亿元,同比增长22.8%,其中益赛普收入5.7亿元(不含外销)(+10.5%),赛普汀实现收入2.3亿元(+41.8%),健尼哌收入0.44亿元(+59.4%),CDMO收入0.64亿元,授权许可收入0.99亿元。2023年正常化EBIDTA为3.0亿元(+279.6%),归母净利润2.9亿元(+497.6%),经营性现金流净额4.2亿元(+78.3%)。截至2023年底,现金储备28.0亿元。
核心管线进展:公司聚焦自免领域,2023年获得多项进展。益赛普预充针于2023年第一季度获批上市;608管线针对中重度斑块银屑病适应症于23年12月达到ph3临床终点,预计24Q4申报NDA,同时拓展放射学阴性脊柱炎和强制性脊柱炎适应症;610管线针对嗜酸性粒细胞哮喘适应症完成ph2入组,预计24年披露临床数据;611管线针对AD适应症在24年1月完成ph3的首例患者入组、针对青少年中重度AD和鼻窦炎适应症处于ph2研究阶段;613管线针对痛风性关节炎的ph2达到终点,预计在24年1月ph3患者入组;621管线针对COPD适应症2023年在中美两地获批,处于ph1研究阶段。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)