2024合成生物学行业报告
合成生物学:异军突起的交叉学科,有目标的改造、设计合成生命体
合成生物学是一门涉及多学科多技术的实用型学科,根据《自然》杂志定义,合成生物学(Synthetic Biology)是设计和建造新的生物部件、设备和系统,以及重新设计现有的自然生物系统,以达到特定实用目的的学科;根据赵国屏院士在关于合成生物学发展的文章中(生物工程学报,2022, 25(11): 4001-4011),对合成生物学的定义阐述,另结合李玉娟等在《合成生物学发展脉络概述》一文中的表述(中国生物工程杂志, 2024, 44(1): 52-60),我们可以认为合成生物学是一个多学科交叉的领域,它以生物科学为基础,融合医学,化学,物理,数学,计算机等学科,采用工程科学的核心研究理念,对生命体进行有目标的改造,设计甚至重新合成,以此来揭示生命运行规律。
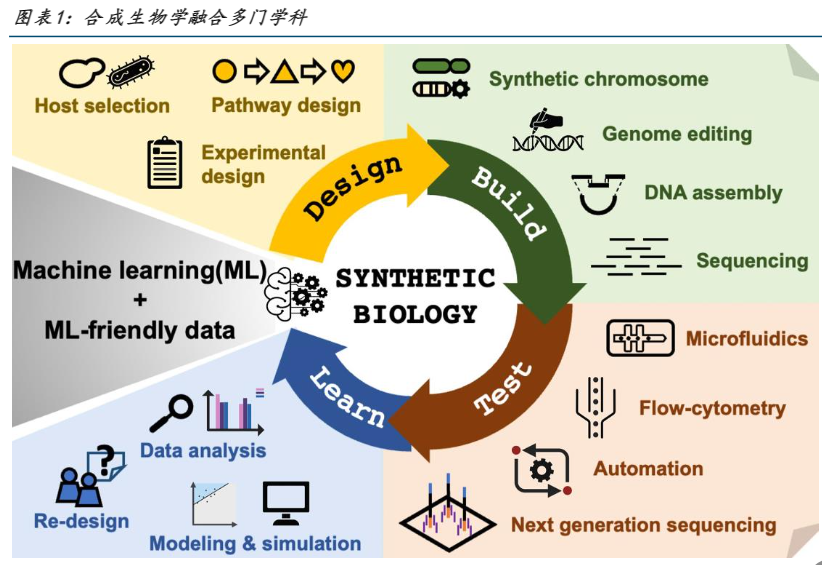
这门新兴学科天然具备工程学科特点,所以有时候称之为工程生物学。它的内涵由学术研究出发,自然迈向应用产业之路,并在加速向绿色制造、健康医药、农业生产、环境保护、生物安全等领域渗透和应用。合成生物学的跨越发展由生命科学技术的进步驱动1953年沃森和克里克发现DNA双螺旋结构(1953),生物学进入了真正的分子时代;1960-1980年代实现蛋白质和核酸的人工合成,合成生物学有了最初期的实践操作;而2000年后随着人类基因组学和分子生物学理论技术的不断成熟,合成生物学作为一个学科逐步成型;而2010年后随着基因编辑、机器学习和人工智能方面的技术取得突破,合成生物学的发展正式进入快车道。
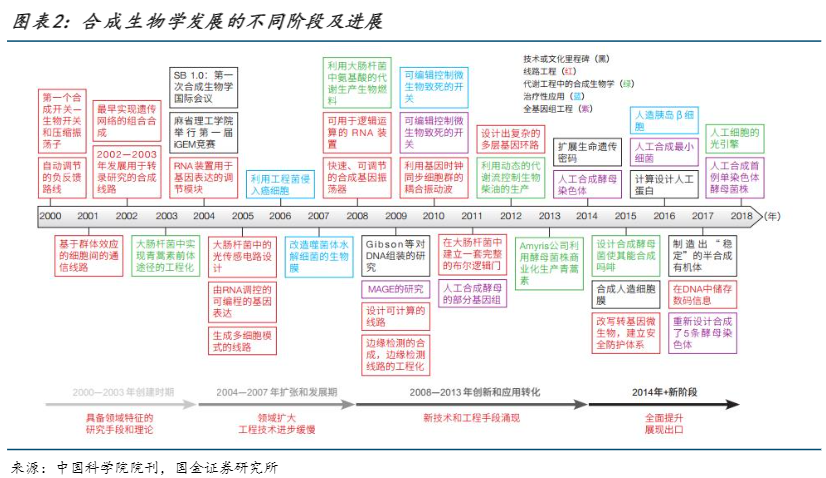
总结以上合成生物学的发展过程可以发现,这个强科技属性的行业每次都是伴随着理论创新和新技术的产生而取得重大突破。合成生物学的各个核心技术环节也与生命科学前沿研究存在密切联系,技术快速迭代。基因合成技术:合成生物学的基础,涉及DNA/RNA的合成。
基因编辑技术:如CRISPR-Cas9,允许科学家精确添加、删除或替换生物体基因。高通量筛选和基因测序技术:自动化的高通量技术能够快速筛选和鉴定合成生物学构建的有效性。蛋白质设计技术:计算机辅助,AI机器学习帮助预测和筛选特定功能蛋白质。生物信息学:利用计算方法分析和解释生物数据,搭建序列到结构和功能的桥梁。合成基因回路:设计能够控制基因表达的复杂回路,类似电子工程中的电路。代谢工程和途径重构:通过修改生物体的代谢途径来增强其生产特定化合物的能力。
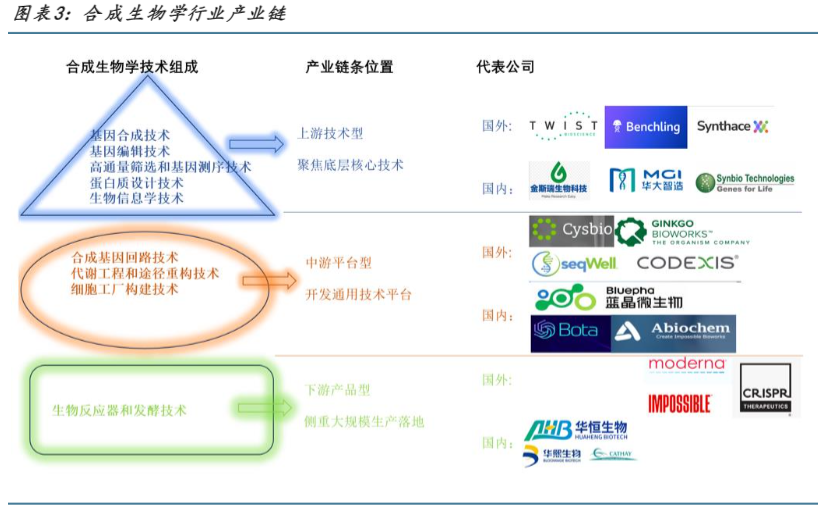
细胞工厂构建:通过将特定的遗传回路和代谢途径整合到底盘细胞中,可以构建出能够生产药物、生物燃料或其他有用化合物的“细胞工厂”。生物反应器和发酵技术:生物反应器提供了适宜的环境条件,以支持细胞工厂的生长和产物的合成,可以大规模生产合成生物学产品。根据合成生物学中用到的相关技术,可以将合成生物学产业链分为上中下游环节:上游-底层技术型,主要集中在基因合成编辑测序等相关核心技术以及组学数据分析解读这方面。国外代表性公司如Twist Bioscience,Synthace和Benchling;国内代表性企业如华大智造,金斯瑞生物科技和苏州泓迅。
中游-平台型,中游为生物体设计开发类的通用型平台。国外代表性公司如Codexis,Cysbio和Ginkgo Bioworks;国内代表性公司如蓝晶微生物,恩和生物和弈柯莱。下游-应用型,下游主要是产品生产应用型,广泛涵盖到了人类生活的方方面面,包括医药,化工,食品,农业等。国外代表性公司如Moderna,CRISPR和Impossible Foods;国内代表性公司如川宁生物,华熙生物,华恒生物,凯赛生物,梅花生物,昊海生科,欣贝莱生物,巨子生物等。
合成生物学在医药、化工、能源等领域存在巨大的应用价值
根据麦肯锡《2021:定义未来的13个趋势》从理论上讲,全球经济中多达60%的实体材料都能利用生物技术生产。合成生物学应用潜力巨大,在实际应用中的核心战略意义是:1.替代传统以石油为终端原料的合成路线,以减少对石油的消耗和环境的污染,这对于传统化工、能源领域尤其重要;2.对部分使用化学合成较为困难的重要产品提供一种成本更低、产量更高、更为简便、环境更加友好的生产路径,这点尤其体现在医药生产和农业领域。值得一提的是,我国“十四五”规划和2035年远景目标纲要中更是明确将合成生物学列为科技前沿领域之一,这体现了国家对这一学科的重视。
合成生物学可为手性药物以及天然产物提高高效、低成本的生产路径手性小分子药物和天然产物的生产是合成生物学在医药领域的重要应用场景:手性药物是医药化学品的重要组成部分,在2022年全球销售额排位前200名的小分子药物中,60%以上是手性小分子药物。目前,通过化学法合成手性医药化学品存在诸如合成步骤复杂或难以合成、催化剂昂贵且易中毒失活、产品ee值低等问题。相比之下,采用生物催化具有条件温和、环境友好、高效、高选择性等优势。目前合成生物学已在多个重磅手性药物的合成中取得突破,其中国内企业弈柯莱生物科技已成功利用生物法实现DPP-4抑制剂西他列汀,HIV药物度鲁特韦中间体的合成,根据BCG咨询的数据,2021年弈柯莱生物科技的收入达3.3亿元,毛利率和净利率分别为37%和9%。
天然产物一直是潜在的先导药物的重要来源,据统计,在近40 年获批上市的药物中,天然产物及其衍生物占1/4。过去来源于植物的天然产物主要依赖传统的植物提取方式进行生产,成本高、周期长,部分植物来源的天然产物还面临植物生长缓慢,且提取难度较大的问题,难以满足社会发展的需求。利用微生物发酵技术可以突破植物资源限制,环境友好、生产速度更快、易于大规模生产。此前青蒿素、吗啡、奥利司他、长春新碱、血管紧张素II等多种经典药物的微生物发酵法路线均已打通。此外,近期重磅抗癌药紫杉醇的生物合成的也取得了重要的突破。2024年来自中国的科学家团队鉴定出了紫杉醇生物合成途径中缺失的关键反应酶,解析了紫杉醇工业化生产前体巴卡亭III生物合成的过程,为利用合成生物学的手段实现紫杉醇的高效合成迈出了关键的一步。
合成生物学在化工领域应用广泛,相比传统石油化工生产路线优势明显目前绝大多数化工材料的终端原材料是石油,而合成生物学可用于解决石油资源日益耗竭以及石油加工中带来的环境污染等问题。除此以外,合成生物技术还可以合成传统化工工艺不能合成的新材料,是一种生产绿色、条件温和且原料广泛的新工艺。目前通过基因工程改造得到的大肠杆菌和谷氨酸棒状菌已被广泛用于PHA、PHB、PLA、戊二胺、丁二酸等传统化学制品的生产。
1,3-丙二醇是一种重要的化工原料,广泛应用于聚酯、聚醚、聚氨酯,以及涂料、去污剂、黏合剂等的合成。过去使用甘油作为原料生产1,3-丙二醇的理论最大转化率只有0.75 mol/mol,致使生成成本过高。杜邦公司首次设计并创建了以葡萄糖为原料的生物合成途径,该途径的底物转化率可达到0.83 mol/mol。基于这一技术,杜邦公司建立了年产4.5万吨1,3-丙二醇的产业化生产线。在提高底物转化率的同时,与传统石化制造路线相比,生物法1,3-丙二醇技术的能耗降低40%,CO2排放减少40%。图表9:生 物合成法合成1,3-丙二醇相比传统石化制造路线优势明显来源:华经情报网,国金证券研究所生物燃料低碳环保,虽离产业化仍有距离但发展趋势清晰生物燃料是以农林废物资源、城市有机垃圾资源等为原料,再通过合成生物技术生产获得的产品,生物燃料具体包括生物乙醇、生物柴油、高级醇等生物液体燃料、生物沼气(甲烷)、生物氢气及生物电等。生物燃料低碳环保,且是各国能源安全的重要选择。与化石能源相比,生物燃料具有可再生性、低污染性,且生物燃料的利用可以帮助人们实现碳中和目标。因此,世界各国均把发展生物燃料视为保障经济发展、能源安全和环境质量的重要战略选择。
生物燃料历史悠久,合成生物学兴起推动其快速发展。早在19世纪后期,生物沼气和生物乙醇实现了工业化的生产;之后在19 世纪70 年代爆发的石油危机导致生物能源发展被广泛关注,客观上加速了各类生物能源研发及产业应用;2000 年以来,随着全球对可持续发展的关注叠加合成生物学逐步兴起和发展,包括纤维素乙醇、高级醇、脂肪烃、生物沼气、生物氢和生物电在内的新一代合成生物能源技术逐步发展。合成生物能源离产业化仍有距离,但趋势明晰。合成生物能源面临:①高昂生产成本和低廉石化产品价值之间的矛盾;②巨大市场需求和技术成熟度较低之间的矛盾,这两个矛盾是合成生物能源产业化推广的关键瓶颈。未来要实现生物资源产业化发展,一方面,需要加强生物能源的原料技术研究、提高转化效率并形成规模化产业优势;另一方面,还需要建立生物质资源从收集、储存、运输到交易的全方位商业模式。
生物燃料市场规模达千亿美元,未来生产技术将成为增加供给的关键。据statista数据显示,预计到2024年全球生物燃料市场规模超过1200亿美元,从2021年至2030年全球生物燃料行业年增长率预计可达5.4%。目前全球生物燃料的生产技术水平依然不高、生物利用度较低,未来随着合成生物学在能源领域的发展将为生物燃料市场空间的拓宽注入更多动力。另外,生物燃料在北美、巴西和欧洲的市场份额最高,分别占据47%、24%和15%。目前我国在全球生物燃料中市场份额有限,未来存在极大的可扩张空间。在美国《通胀削减法案》等各国法规和政府补贴的刺激下,生物能源产量正在强劲增长。据芝加哥商品交易所发布的研究显示,通过新建生产设施和改造石油炼厂,美国可再生柴油产能在2021年至2023年期间增长了两倍,而且到2025年有望进一步翻番,达到每年1740万吨。另外欧洲的氢化植物油(HVO)预计也将呈现类似趋势,而生物能源的快速增长势头甚至蔓延到了生物柴油和可持续航空燃料领域。
合成生物学应用多方位提高粮食产量,为稀缺营养物质提供廉价替代的可能传统策略提升粮食产量有限,加速合成生物农业推广。农业领域又可分为育种、作物保护、作物营养等赛道,而在该领域的主要关注点在于两个方面:提高产量和增加营养价值。之前人们通过大规模开发合成和天然肥料、优化育种等策略,旨在最大限度地改善植物结构和提高植物光合作用利用率,以获得更高的产量。但以上传统的农业策略更侧重于个体成分的调控、难以实现提升营养的目标、且导致农业排放中的甲烷及氮氧化物占比较高,不利于环境保护。随着合成生物学在农业领域的逐渐推广,其在减少肥料使用、减少碳排放、强化病害防控、提高生长效率等方面的优势日益凸显。目前合成生物学已然在部分设计育种、固氮肥料和微生物农药已实现商业化。以育种为例,合成生物学应用主要分为三类:①通过野生植物驯化,提升产量和质量;②提高果实质量、固氮、抗虫抗药等性能改造;③通过合成生物学来促进羧化反应,提高光能利用,降低光呼吸损失。另外从技术角度,相比传统育种技术,基因编辑在新作物开发、性状开发等方面具有目标明确、成本更低、耗时更短等明显优势。以微生物农药为例,合成生物学还可用于新型农药开发,包括RNAi/微生物农药和植物源农药,这类农药的除虫效率将更高。
合成生物学为稀缺营养物质提供廉价替代的可能。在农业领域需要提高作物的营养价值以解决营养不良的问题,合成生物技术能够产生一系列人体需要且稀缺的营养物质、并提高人类的健康水平。例如,维生素A缺乏会导致严重的健康问题,这在以大米为主食且食物多样性有限的国家尤为突出。而植物烯合成酶和胡萝卜素去饱和酶两个类胡萝卜素的生物合成基因,可以诱导水稻中β-胡萝卜素(维生素原A)的合成和积累,以解决维生素A的缺乏。另外还有几种类胡萝卜素及其含氧衍生物—叶黄素、长链多不饱和脂肪酸(VLC-PUFA),这些营养物质主要与人类的眼睛、心血管健康、功能性免疫系统、认知功能以及抗氧化活性等健康益处相关,未来在合成技术的支持下,这些营养素将会有廉价的替代品。
政策端:海外各国政府积极推进合成生物学发展,国内政策红利助力产业发展
美国:合成生物学的领跑者,总统行政令推动生物技术发展全球维度而言,美国属于较早发展合成生物学的国家。2006年美国成立合成生物学工程研究中心(Synberc),并由美国国家自然基金会(NFS)为其提供10年3900万美金的资助用以推动合成生物学的发展。在NSF 支持的10 年中,Synberc通过成员实验室的研究、学术界和行业成员之间的互动以及支持社会责任创新的广泛影响的活动,为合成生物学领域的发展做出了重要的早期贡献。2022年9月,美国总统拜登签署了一项启动“国家生物技术和生物制造计划”的行政命令,以促进美国生物技术创新、提升生物制造能力。同月,白宫主办国家生物技术和生物制造峰会,各政府部门和机构宣布投入20余亿美元推进该计划。总统行政令加速推动了美国生物技术的发展。
欧洲:主要大国持续加强生物技术政策驱动2020年1月,德国联邦政府内阁正式通过了由德国联邦教研部和农业部两部委主导、联合其他部委提出的《国家生物经济政策战略》,德国两部委承诺将在2020年至2024年期间生物经济领域的预算将达到36亿欧元。此外德国国家生物经济战略的具体目标还包括:1)推动生物技术的研究;2)提高生物基础的经济在整个国民经济的比重;3)强化高分子遗传研;4)制订具体财政预算来支持生物经济等。英国在合成生物学机遇下做出积极响应,分别于2012年、2016年、2018年及2019年发布多份合成生物学战略计划。2012年的《英国合成生物学战略路线图2012》中,总结了英国合成生物学发展的5 个关键建议,分别为:1)建设多学科网络中心,构建英国合成生物学资源体系;2)建立英国合成生物学社区;3)促进技术市场化;4)形成国际领导地位;5)建立领导理事会。同时英国政府围绕合成生物发展路径进行布局,其在2012 年底成立了英国合成生物学领导理事会(SBLC),进一步深化对合成生物学的布局。法国整体在合成生物学政策上支持与争议并行,如法国出台了《国家研究与创新战略》、《国家研究战略:法国-欧洲2020》、《法国国家生物生产战略》、《法国健康创新2030 战略》等驱动政策。但合成生物学的发展也同样受制于法国相关机构对于生物风险等伦理安全的争议。
中国:生物技术的发展及应用逐步被纳入国家战略计划中国制定了一系列政策文件和规划,支持合成生物学在生物制造、医药、能源等领域的应用。例如早在2011年,国家科技部在《“十二五”生物技术发展规划》中提及,生物技术是国际科技发展的主要推动力,同时也成为国际竞争的焦点。因此,国家科技部将合成生物学技术列为重点需要突破的核心关键技术之一。近年随着生物技术的发展,国家陆续加强对于合成生物学的关注,《2024年国务院政府工作报告》中再次提及,要加快发展新质生产力,加快前沿新兴氢能新材料、创新药等产业发展,积极打造生物制造、商业航天低空经济等新增长引擎。目前我国生物制造产业正处于政策红利期。
合成生物学核心技术:构建底盘细胞和放大生产规模
合成生物学的核心技术是底盘细胞的构建和生产规模的放大。现在合成生物学的起点通常利用基因工程技术对特定的细胞进行改造,使其具有合成某种特定物质的能力,随后将细胞进行扩大培养,之后发酵等工艺进行大规模的生产。发酵工艺应用时间较长,技术门槛相对较低,因此底盘细胞的构建成为了合成生物学技术的主要壁垒。近年来,随着基因测序,基因合成和基因编辑技术取得重要突破,合成生物学也得到了快速的发展。基因测序,基因合成和基因编辑技术是构建底盘细胞也是推动合成生物学进步的核心合成生物学的基础是构建合适的底盘细胞。底盘细胞是可用于合成特定物质的宿主细胞。
出于基因信息明确,易于改造,饲养成本低等原因,一般以大肠杆菌,乳酸乳球菌,谷氨酸棒杆菌,酵母等细菌或者真菌细胞做为宿主细胞。研究人员需要结合的具体合成目标选择合适的宿主细胞。菌种的改造和高效的工业化大生产工程能力是合成生物学产业化成功的关键因素,根据华恒生物招股书,生物法大部分反应步骤均在微生物或酶的作用下进行,菌种自身的性能如效率和鲁棒性很大程度上决定了其是否适合产业化。
改造底盘细胞,使优化的底盘细胞增加重构途径中的物质和能量供应,减少细胞内源的消耗、杂质的生成,解除引入产物对细胞的反馈抑制或毒性作用,使菌种具有更好的操作性、鲁棒性,这些策略都是实现高效生物制造的关键。此外,生物制造一般会经历更为严格的小试、中试、放大过程,去探索不同条件下最优的生产条件、工艺参数、设备选型等,这些对大规模、低成本生产极为重要。在底盘细胞构建的过程中,基因测序技术主要用于关键生物酶的基因序列的测序以及检测宿主细胞是否被正确改造。基因合成技术主要应用于合成编码关键生物酶的基因片段,基因编辑技术则主要用于对宿主的基因组进行改造。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)