2024医药生物行业周报:IVD出海机遇与企业推荐
1.1. 医药估值极具有吸引力,重点推荐中药OTC及创新药
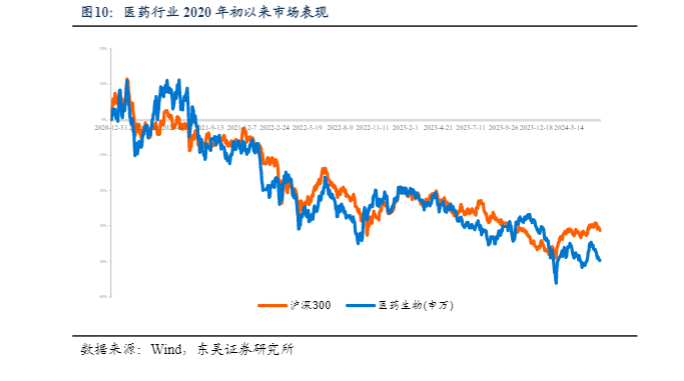
本周、年初至今医药指数涨幅分别为-0.94%、-13.6%,相对沪指的超额收益分别为-0.34%、-17.94%;本周化药、生物制品及医疗器械等股跌幅较小,中药、商业及医疗服务等股价跌幅较大;本周涨幅居前欧林生物(+19.48%)、天益医疗(+16.78%)、东诚药业(+13.30%),跌幅居前圣达生物(-13.67%)、欧康药业(-13.02%)、共同药业(-12.31%)。涨跌表现特点:本周医药板块连续下跌三周、大小市值个股普跌,其中中药跌幅领先。
2.1. IVD是医药板块中出海潜力领先的板块
根据沙利文数据,2022年全球IVD市场规模约为907亿美元,2017-2022年保持约7%的增速稳定增长。分地区看,亚太、拉美等新兴市场IVD行业增速比欧美日韩等成熟市场明显更快。尤其是印度、俄罗斯、越南、巴西等成本敏感却本地IVD企业落后的国家,是我国IVD出海的主要市场。
目前我国已有大量高出海比例的IVD企业,其中九安医疗等海外收入占比超过90%,出海比例高的企业主要出口胶体金等技术含量较低的品种。以新产业、迈瑞为首的化学发光企业在加速出海,其中新产业海外业务比例已占30%以上,且保持30%左右的稳定高增速。
IVD出海主要地区在俄罗斯、印度、东南亚、南美等地区,这些地区逐渐开始技术迭代(例如免疫学中从ELISA等逐步替换到化学发光),考虑到经济性,国产企业在本轮产业升级中有优势。建议关注具备先发和平台优势的企业,推荐新产业、迈瑞医疗等,关注九安医疗、万孚生物等。
2.2. 公共卫生事件后诊疗量回升,反腐影响边际减弱
化学发光是我们最看好的版块之一,是目前行业增速最快的子行业。2019年化学发光市场规模为221亿,2015-2019年CAGR高达22.71%,预计市场规模将在2030年达到1035亿元,2019-2030年CAGR为13.73%。
进口品牌寡头垄断,国产替代趋势清晰。从竞争格局看,进口品牌罗氏、雅培、贝克曼和西门子市占率具有绝对优势,四者市占率合计超75%,但呈现逐年下降趋势,国产化率由2019年的23%上升至2021年的27%。国产品牌中新产业、安图、迈瑞和迈克逐渐凸显,未来3-4年有望完成市占率25-30%到50-60%的提升。
公共卫生事件后诊疗量快速恢复。我国基层医院与三级医院诊疗量巨大,2019年基层医院诊疗量为40.4亿人次,三级医院诊疗量为17.7亿人次。2019年公共卫生事件发生后,基层医院与三级医院诊疗量急速下滑至2020年的22.9亿人次与15.6亿人次。随着后续政策逐渐宽松,诊疗量逐步回升。2023年彻底放开后诊疗量分别回升至22.3亿人次和23.3亿人次,同比分别增长12.11%和14.64%,恢复趋势显著。我们预计随着全国生产生活恢复常态化,医院诊疗量将进一步回升至2019年前水平。IVD作为企业收入与诊疗量强相关的板块,有望受益于诊疗量恢复。
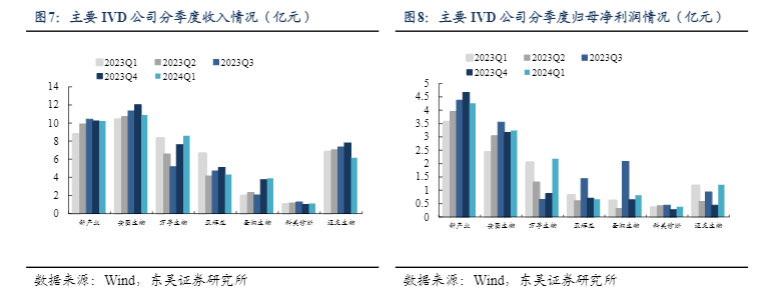
反腐边际影响减弱,2024Q2转折点出现。IVD板块在2023H2短期受到反腐影响,试剂使用量和设备入院均受影响。主要IVD企业2023Q3、2023Q4、2024Q1业绩均有所下滑或增速放缓。目前反腐边际改善,学术会议开始恢复,主要IVD企业虽然2024Q1收入端环比仍有所下滑,但利润端拐点已现,环比转增。我们预计业绩将在2024Q2环比加速,IVD常规业务将在2024年迎来全面恢复。
2.3. DRGs加速国产替代,国产品牌性价比凸显
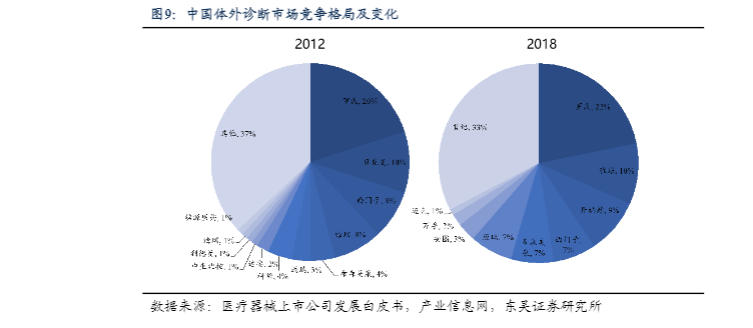
DRGs倒逼医院进行成本管控,高性价比国产品牌迎来机遇。DRG 等医保支付方式改革持续推进。政策要求2021 年年底:30 DRG+71 DIP 试点进入实际付费。支付方式改革在2022-24 年的覆盖医疗机构不少于40%、30%、30%,按疾病诊断分组和按病种付费/住院费用达70%,2025 年实现机构、病种、基金全覆盖。DRG/DIP 改革后,医疗机构将加强成本管理,提高医保基金的使用效能,高临床价值的药品、器械和技术难度较高的服务项目仍将得到资源倾斜,价格虚高、临床价值不明确的项目将被挤出水分。DRGs 主要将医疗带回循证医学,其中检测质量和成本是关键。医保控费及药品零加成背景下,公立医院“以药养医”的医疗体制逐步发生变化,开始回归医学本质“循证医学”。目前公立医院的结余主要来自于检验科、影像、病理等医技科室。公立医院对检验科成本管控、质量管理越来越重视。目前我国IVD行业头部为进口企业,2018年市场CR5全部为进口品牌,合计市占率55%,较2015年50%有一定提升,主要系进口品牌加大新兴国家市场投入,主流赛道加速新产品放量所致。国产品牌中迈瑞(IVD部分)、安图、万孚市占率增长显著,2018年分别达7%、3%和2%。相较进口品牌昂贵的价格,国产品牌的高性价比在医保控费大背景下更受医院青睐。
3.1. 创新药/改良药研发进展(获批上市/申报上市/获批临床)
诺和诺德宣布,欧盟委员会(EC)已给予Awiqli(基础胰岛素周制剂依柯胰岛素insulin icodec)上市授权,用于治疗成人糖尿病患者。
5月27日,NMPA官网显示,琅铧医药引进的盐酸替洛利生片(Pitolisant)获批新适应症,用于治疗发作性睡病青少年和6岁以上儿童患者的日间过度嗜睡(EDS)或猝倒。
5月29日,罗氏宣布其PI3Kα抑制剂Inavolisib(GDC-0077)的新药申请(NDA)已被FDA受理并获优先审评资格,用于联合哌柏西利和氟维司群治疗既往接受内分泌疗法辅助治疗后或完成辅助内分泌治疗后12个月内复发的PIK3CA突变、激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)的局部晚期或转移性乳腺癌成人患者,PDUFA日期定为2024年11月27日。
5月29日,Tris Pharma宣布FDA已经批准ONYDA™XR(盐酸可乐定)上市,用来单药治疗或者辅助中枢兴奋剂药物治疗6岁及以上注意力缺陷多动症(ADHD)患者。这是FDA批准的首款也是唯一一款液体非兴奋剂类ADHD药物。
5月30日,BMS宣布FDA已经批准Breyanzi(lisocabtagene maraleucel,liso-cel)用于治疗复发或难治性套细胞淋巴瘤(MCL)成人患者,这些患者既往接受过至少两种全身治疗,包括一种BTK抑制剂。
3.2. 仿制药及生物类似物上市、临床申报情况
5月28日,CDE官网显示,博安生物度拉糖肽注射液(BA5101)上市申请已获受理,用于成人2型糖尿病患者的血糖控制。这是国产首款申报上市的度拉糖肽生物类似药。
3.3. 重要研发管线一览
5月27日,第一三共与阿斯利康共同宣布,针对III期TROPION-Lung01研究的结果更新表明:相较于多西他赛,Datopotamab deruxtecan(Dato-DXd)在既往至少接受过一线治疗的局部晚期或转移性非小细胞肺癌(NSCLC)非鳞癌患者中,展现出了总生存期(OS)结果的临床意义改善。
药物临床试验登记与信息公示平台显示,阿斯利康在中国登记了齐泊腾坦(zibotentan)/达格列净复方治疗慢性肾脏病伴高蛋白尿的III期、随机、多中心、双盲研究。
5月28日,信达生物宣布其自主研发的重组抗白介素23p19亚基(IL-23p19)抗体匹康奇拜单抗(研发代号:IBI112)在中国中重度斑块状银屑病受试者中开展的III期临床研究(CLEAR-1)达到主要终点和所有关键次要终点。信达生物计划向CDE递交匹康奇拜单抗新药上市申请。
5月29日,泽璟制药宣布盐酸吉卡昔替尼片(曾用名:盐酸杰克替尼片)用于治疗12岁及以上青少年和成人非节段型白癜风患者的II/III期临床试验获批。
5月28日,默沙东宣布代号为KEYNOTE-522的关键III期临床研究达到总生存期(OS)终点。在独立数据监测委员会进行的预先指定的中期分析中,与单纯术前化疗相比,Keytruda(帕博利珠单抗)联合化疗作为新辅助治疗,术后继续单药作为辅助治疗可使高危早期三阴性乳腺癌(TNBC)患者OS显示出具有统计学意义和临床意义的改善。
5月28日晚间,康宁杰瑞发布公告,称其PD-L1/CTLA-4双抗KN046联合白蛋白紫杉醇及吉西他滨对比安慰剂联合白蛋白紫杉醇及吉西他滨用于治疗未接受系统性治疗的不可切除局部晚期或转移性胰腺导管腺癌(PDAC)的III期KN046-303研究总生存期(OS)结果未达到预设的统计学终点。
5月29日,强生宣布其first in class选择性人类食欲素2受体(OX2R)拮抗剂Seltorexant(JNJ-42847922)辅助治疗重度抑郁症(MDD)患者的III期MDD3001研究达到了所有的主要终点和次要终点。
5月28日,药物临床试验登记与信息公示平台显示,恒瑞医药自主研发的抗IL-4Rα单抗SHR-1819启动III期临床试验,成为了第8款进入III期阶段的国产抗IL-4Rα单抗。
5月30日,荣昌生物(股票代码:688331.SH / 09995.HK)宣布,维迪西妥单抗被中国国家药品监督管理局(NMPA)药品审评中心(CDE)正式纳入突破性治疗药物品种,针对适应症为:维迪西妥单抗联合特瑞普利单抗围手术期治疗存在HER2表达且计划进行根治性膀胱切除术的肌层浸润性膀胱癌(MIBC)。
近日,根据clinicaltrials.gov网站显示,诺华将撤回(Withdrawn)KRAS G12C抑制剂JDQ443(opnurasib)的一项II期STRIDER研究(NCT05999357),原因是诺华已终止opnurasib的开发。该项研究旨在评估opnurasib在KRAS G12C突变NSCLC脑转移患者中的颅内疗效,原本预计于今年4月15日启动,于2027年8月完成主要研究内容。
5月30日,Soterios Pharma宣布,其非甾体类局部疗法STS-01治疗轻度/中度斑秃的II期研究取得了积极结果。据公司新闻稿,STS-01有可能成为第一个获批的轻度/中度斑秃疗法和护理标准。
5月30日,吉利德宣布Trop 2 ADC Trodelvy(戈沙妥珠单抗)对比化疗(医生选择的治疗,TPC)用于先前接受过含铂化疗和抗PD-(L)1治疗的局部晚期或转移性尿路上皮癌(mUC)患者的确证性III期TROPiCS-04研究未达到总生存期(OS)主要终点。
5月31日,康方生物宣布,全球首创双特异性抗体新药依沃西单抗(PD-1/VEGF双抗)单药对比帕博利珠单抗一线治疗PD-L1表达阳性(PD-L1 TPS≥1%)的局部晚期或转移性非小细胞肺癌(NSCLC)的注册性III期临床研究(HARMONi-2或AK112-303),由独立数据监察委员会(IDMC)进行的预先设定的期中分析显示强阳性结果:达到无进展生存期(PFS)的主要研究终点。
本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。