2024血液制品行业报告:市场扩容与产品创新双驱动
1.血液制品批签发增量明显,“十四五”新增浆站弥补供给缺口
1.1行业监管严格,原料血浆具有稀缺性
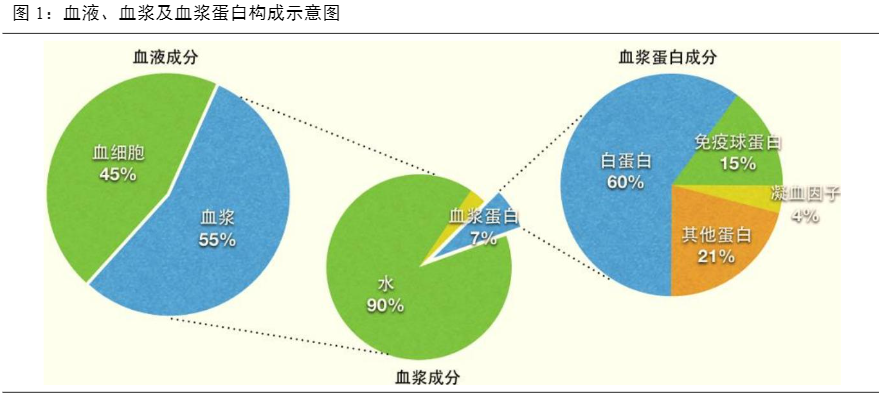
血液制品是将血液中不同的蛋白组分分离后制备的各种产品。人体血液中血浆约占55%,血浆中又有约90%是水,7%是蛋白质。蛋白质中约60%为白蛋白、约15%为免疫球蛋白、约4%为凝血因子类、约21%为其他蛋白成分。
血液制品行业具有较高的政策壁垒。国家在血液制品行业准入、原料血浆采集管理、生产经营、产品进口和价格等方面制定了一系列监管和限制措施。国家对血液制品生产企业实行总量控制,自2001年5月起不再批准新的血液制品生产企业。
国内正常经营的血液制品企业不足30家,企业扩张只能通过并购或新设采浆站两种方式。浆站设立上,国家规定,自治区、直辖市人民政府卫生行政部门制定区域内单采血浆站设置规划和采集血浆的区域规划。单采血浆站应当设置在县(旗)及县级市,不得与一般血站设置在同一县级行政区域内;一个采血区域内只能设置一个单采血浆站。
单采血浆站只能向一个与其签订质量责任书的血液制品生产单位供应原料血浆,严禁向其他任何单位供应原料血浆。血液制品生产单位注册的血液制品少于6个品种的,承担国家计划免疫任务的血液制品生产单位少于5个品种的,不得设立单采血站。
申请设置单采血浆站的,由县级人民政府卫生行政部门初审,经设区的市、自治州人民政府卫生行政部门或者省、自治区人民政府设立的派出机关的卫生行政机构审查同意,报省、自治区、直辖市人民政府卫生行政部门审批;经审查符合条件的,由省、自治区、直辖市人民政府卫生行政部门核发《单采血浆许可证》。
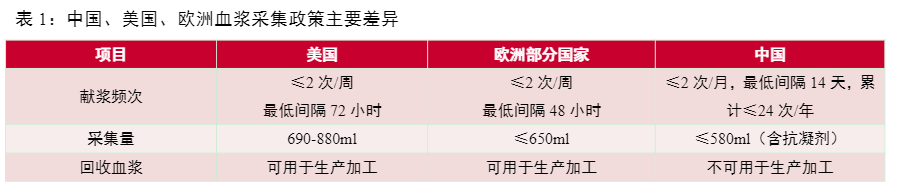
按规定,献浆员只能在户籍地划定采浆区域的单采血浆站献血浆,不能跨区域献浆或者流动献浆。两次献浆间隔不得少于14天,一年内累计献浆次数不得超过24次,每次献浆量不得超过600克(含抗凝剂,以容积比换算不超过580ml)。总采浆量成为血制品企业核心竞争力之一。我国对进口血液制品同样采取严格管制,1985年开始国家禁止除人血白蛋白以外的血液制品的进口,2002年起禁止从疯牛病疫区进口人血白蛋白。
为了缓解凝血因子VIII供应紧张的局面和满足血友病患者的用药需求,2007年11月开始允许进口重组类人凝血因子产品。除上述之外,国家对血液制品实行批签发制度,每批制品出厂上市或者进口时需进行强制性检验、审核。同时,血液制品的价格也受到严格的限制。
1.2中国血液制品种类数量和人均使用量与国外有较大差距
创伤性、出血性休克、严重烧伤及低蛋白血症,在中风、肝硬化和肾病等常见疾病中有广泛应用。免疫球蛋白产品用于免疫球蛋白缺乏症、自身免疫性疾病以及各类感染性疾病的治疗,与抗生素或抗病毒药合用可提高对某些细菌性或病毒性感染疾病的疗效;凝血因子产品用于治疗各种凝血障碍类疾病及外科手术止血。我国血液制品人均血液制品使用量与发达国家均有较大差距。从消费结构上看,国内主要的消费在人血白蛋白,欧美发达国家免疫球蛋白和凝血因子类产品的平均消费量远高于我国。我国白蛋白人均使用量不足美加日的1/5,免疫球蛋白不足1/4,凝血因子更是不足1/50。
我国血液制品可提取14种,有超过10种产品待上市。目前,CSL(杰特贝林)、武田等国际巨头能从血浆中通过层析等技术方法,提取20多种蛋白因子,国内血液制品企业品种最多提取14种。相比美欧日,国内血浆的综合利用效率偏低,品种上呈现结构性供应不足,有很大的优化空间。国内蛋白酶抑制剂类尚未上市,凝血因子可提取品种较多,国内有5种品种尚未上市,包括凝血因子类的C蛋白浓缩物、凝血因子X、因子IX复合体、凝血因子VIII/血管性血友病因子复合物、抗抑制剂凝血复合物(APCC)。免疫球蛋白中皮下注射人免疫球蛋白尚未有上市产品。特异性免疫球蛋白有6款产品尚未上市,包括静脉注射炭疽免疫球蛋白、静脉注射肉毒杆菌免疫球蛋白、巨细胞病毒免疫球蛋白静脉注射、RhO(D)免疫球蛋白静脉注射、静脉注射疫苗免疫球蛋白、水痘带状疱疹免疫球蛋白。
1.3“十四五”新设浆站陆续投产,采浆量有望持续增加
国内血浆供应缺口较大,十四五”单采血浆站陆续投产,预计带动国内采浆量增加。中国血液制品市场规模稳定提升,中商情报网数据显示,我国血液制品市场规模由2018年283亿元增长至2022年的408亿元,CAGR为9.58%。根据博雅生物公告,国内原料血浆需求量已超16000吨/年,而2023年国内单采血浆站共采集血浆约12,079吨(+19%),国内原料血浆供应量快速增长。十三五期间,浆站审批趋紧增速放缓,到2020年主要上市血制品企业在营浆站总计达到167家。十四五期间,各省加大新设单采浆站,2023年上市血制品企业浆站达到217家,增幅30%。浆站建成后有望有效带动采浆量的增加,满足供需缺口。

2.白蛋白进口替代空间较大,免疫球蛋白增长潜力十足
23年血液制品批签发改善明显,人血白蛋白、静丙、人凝血因子VIII增速显著。从22年二季度开始我国血液制品批签发次数明显恢复,根据中检院数据,23年Q2血液制品主要品种批签发1640次(+18.8%),人血白蛋白、静丙、人凝血因子VIII批签发为995次(+13.1%)、285次(+27.8%)、102次(+29.1%)。
2.1白蛋白市场持续增长,国产替代空间较大
人血白蛋白是血浆中主要的蛋白质,生理功能广泛。白蛋白是血浆中含量最高的蛋白质,可以维持渗透压和体液平衡,抗休克作用,运输和解毒作用,能调节水肿、腹水,还可供给营养。根据《人血白蛋白临床应用及处方点评分析》,人血白蛋白使用量前十的科室是肿瘤科、消化内科、心胸外科、感染科等,其中肿瘤科用药人数占到了14.45%。
人血白蛋白价格整体较为稳定,市场持续增长。人血白蛋白药品的价格维持在380元(50ml:10g规格)左右,2022年广东11省集采中对价格影响较小。人血白蛋白应用广泛,市场持续增长,根据弗若斯特沙利文数据,2023年人血白蛋白药用市场规模预计达到361亿元,到2025年市场有望达到421亿元。
进口厂商主导人血白蛋白市场,国产替代空间较大。2001年后国内无新批血液制品生产企业,血浆供给短缺导致人血白蛋白药品存在较大的市场缺口。根据中检院批签发数据,2023年进口人血白蛋白占比64.38%,我国人血白蛋白严重依赖进口。随着后续国产人血白蛋白批签发的增长,国产有望对进口人血白蛋白实现替代,国产厂商华兰生物、国药集团、泰邦生物、上海莱士有较大的增长空间。
2.2全球免疫球蛋白市场稳定增长,大品种静丙需求旺盛
全球免疫球蛋白用量稳定增长,用药人数持续增加。人免疫球蛋白制品(IgG)已使用50余年,它包括普通人免疫球蛋白和超免疫或特异性免疫人免疫球蛋白。免疫球蛋白的使用呈增加趋势,根据《DATA&ANALYSISOFIMMUNOGLOBULINSUPPLYANDPLASMAREQUIREMENTSINEUROPE2010-2021》,全球免疫球蛋白消费量以平均每年8%的速度增长。全球人群的免疫球蛋白消费和支出显著增加。
静丙(静注人免疫球蛋白)的适应症有较大的提升空间,市场增长潜力较大。样本医院静丙销售金额呈稳定上升态势。药智网数据显示,2022年静丙销售金额为65.76亿元。《中国血液制品发展与临床应用蓝皮书》数据显示,目前国内静丙获批适应症较少,美国FDA批准的IVIG9大类适应症,而我国适应症获批则仅有6个,主要集中在免疫疾病和抗感染领域,适应症有较大提升空间,国内对于静丙的认知度有提升潜力,新冠疫情很大程度上提升了医生、患者对血液制品的认知,市场需求量较前期有明显提升。随着国内对于血液制品的认知提升及产品的适应症范围的扩大,人均用量将会得到大幅提升。
2.3出血性疾病市场稳定增长,重组凝血因子VIII有望国产替代
全球出血性疾病稳定增长,重组凝血因子占比过半。全球出血性疾病药物市场分为血友病A、血友病B、血管性血友病等。参与血液凝固的凝血因子蛋白有十三个,病理情况下机体由于缺乏某些凝血因子而造成出血。凝血因子缺乏病补充治疗应根据所缺乏的凝血因子来选择特定的凝血因子浓缩剂。
凝血因子浓缩剂已广泛用于治疗先天性缺乏这些凝血因子的患者,血友病A型疾病是出血性疾病类型中最常见的疾病,根据RESARCHANDMARKET数据,由于全球人口对血液疾病的关注日益增加,预计全球出血性疾病药物市场将以8.44%的复合年增长率增长,到2026年将达到240亿美元。重组凝血因子在2020年以52.91%的市场份额主导了全球出血性疾病用药市场。
我国血友病患者众多,预计用药市场持续增长。血友病是出血性疾病的主要类型,根据弗若斯特沙利文数据,2019年中国血友病患者人数达到14万人,甲型血友病占血友病总患病人数的80%~85%,预计到2030年底中国血友病患病人数预计将达到14.6万人。预计2023年中国血友病用药市场达到55.2亿人民币,2030年达到141.0亿元,年复合增长率14.3%。
国产重组凝血因子有较大替代空间。观研报告网数据显示,2022年我国凝血因子市场规模为34.16亿元。国内凝血因子类主要产品为人凝血因子VIII、人凝血酶原复合物和人纤维蛋白。重组类凝血因子国家开放进口,进口厂商更有优势,根据药渡网数据,注射用重组人凝血因子VIII国内有5家进口厂商,3家国产厂商,注射用重组人凝血因子VIIa、注射用重组人凝血因子IX均只有进口厂商上市,说明重组凝血因子的国产上市将带来国产替代。
国产重组人凝血因子VIII逐步上市。中国血友病市场可以区分为血源性人凝血VIII因子和重组人凝血VIII因子两部分。很多成熟市场血友病的治疗需求由安全性有效性更高且不依赖于血浆供应的重组人凝血VIII因子满足。近年来中国重组人凝血因子的份额一步步提高,向着成熟市场的产业结构靠拢。目前国内重组人凝血因子VIII已获批上市的主要国产厂家包括神州细胞、正大天晴和天坛生物。
3.并购整合浆站实现外延增长,新浆站、新品种保障内生增长
3.1血制品行业呈现寡头垄断,国内国资主导行业并购整合
全球血液制品行业呈寡头垄断格局,市场占有率、浆站数量以及采浆占比高度集中。全球血液制品企业,数量从20世纪末100多家到目前不到20多家(不含中国),其中美国5家,欧洲8家,基立福、杰特贝林、奥克特珐玛、武田主导全球市场。全球有上千家单采血浆站,血浆采集量约6万吨;其中近70%设置在美国,10%在欧洲。基立福(GRIFOLS)、杰特贝林(CSL)、奥克特珐玛(OCTPHARMA)、武田的浆站数量占到全球浆站数量的近70%,采浆量达到70%以上。按全球血制品市场300亿美金计算,杰特贝林(19.9%)、武田(19.8%)和基立福(17.6%)占领了全球近六成的市场。
国内血液制品内部整合,外延并购加速发展。国内血液制品企业经过行业大量并购、重组后,截至目前维持正常生产经营的企业约28家。近年国资参与血液制品行业的整合,多家主要血制品企业被国资收购,后续有望借助国资背景加强血制品业务。
3.2单站采浆量和吨浆收入行业差异大,浆站经营效率是关键
国内集中度较高头部效应显著,新设浆站开发带来增量。国内血制品行业形成了以天坛生物、上海莱士、华兰生物、派林生物为行业龙头的竞争格局,2023年前四家公司采集血浆量都计在1000吨以上,合计采浆占国内血浆采集量60%,头部效益明显。血液制品行业供给端增长主要来自于新设浆站和已有浆站的开发,天坛生物2020年-2023H1在营浆站新增20多家,华兰生物和派林生物20-22年新增浆站也较多。
已有浆站采浆效率、吨浆利用仍有较大提升空间。各企业单站采浆量与单吨收入差异较大,单站采浆量平均在33-57吨/站之间,单吨收入在130-311万元/吨之间。华兰生物单浆产浆达到42吨/站,采浆效率较高。博雅生物有着最高的单吨收入,22年达到311万元/吨,单吨收入的不同与血制品企业的产品结构有关。未来随着浆站采浆效率提升、吨浆利用提升,血制品企业效益也有较大提升空间。
3.3血液制品企业品种逐步丰富,高浓度静丙等品种陆续上市
国内血液制品企业品种逐步丰富,有望产生更多大品种。天坛生物是我国血液制品行业中品种较多、规格较全的企业之一,天坛生物、上海莱士、华兰生物、派林生物分别有血液制品品种14、12、11、11种。国内血液制品企业布局多种血液制品产品研发,根据药智网数据显示,天坛生物、山东泰邦有近十个管线。其他企业也有品种在临床中。其中高浓度静丙、重组凝血VIII因子已经上市,已经进入临床的新品种有多款,包括C1酯酶抑制剂、人凝血因子IX、静注炭疽人免疫球蛋白。
四代层析静丙上市,四代静丙治疗效果相似,住院时间明显缩短。上世纪60年代,欧洲浓度为3%的第一代静丙上市;上世纪90年代,成都蓉生在国内推出浓度为5%的第三代静丙,23年9月天坛生物子公司成都蓉生的国内首个第四代静注人免疫球蛋白——“蓉生静丙®10%”正式获批上市。四代层析静丙相比于国内5%浓度的传统三代静丙,在蛋白纯化、病毒灭活、产品配方等方面更优,临床使用更加安全高效。输注四代层析静丙单次输注时间明显缩短,住院时间明显缩短,住院期间导致不良反应的风险因素显著减少。药代动力学分析表明静丙10%和5%在28天给药间隔下具有生物等效性。静丙10%制剂在儿童和成人受试者中安全且耐受性良好。
国产重组人血白蛋白进入临床3期,安全性良好,预计上市后解决国内白蛋白短缺问题。目前,全球市场上只有通过血浆提取得到的人血白蛋白药品,全球市场尚未有重组人血白蛋白上市药品在售。人血白蛋白使用剂量高、用量大,对安全性、成本、规模化生产要求高,是国际上的技术难题。在研的重组人血白蛋白药品数量较少,药智网数据显示,禾元生物、安睿特的重组人血白蛋白已经进展到3期临床。一项重组人血白蛋白和人血白蛋白临床I期对比的实验表明重组人血白蛋白耐受性良好,AE发生率相似,安全性和重组人血白蛋白相似。如果重组人血白蛋白产品上市,预计将解决国内白蛋白资源短缺和血浆来源人血白蛋白病原体的传播的风险,有良好的应用前景。
4.相关公司概述
4.1基立福(GRIFOLS):采浆量恢复带动静丙增长,皮下注射免疫球蛋白需求旺盛
2023年基立福生物药收入55.6亿欧元(+11.0%),免疫球蛋白及白蛋白业务带动业绩持续增长。基立福浆站数量已经超过380家,得益于采浆量和下游血液制品需求的恢复,免疫球蛋白收入增速达到15.8%。中国白蛋白需求旺盛带动基立福白蛋白业绩持续增长。
4.2杰特贝林(CSL):疫情后采浆量大幅提升,免疫球蛋白增长亮眼
23年,CSL新开12家血站,浆站数量达到342个,叠加疫情后采浆恢复,23年公司采浆量增加31%。根据CSL年报,23年CSL免疫球蛋白收入达到46.75亿美元。2023年PRIVIGEN®(静脉注射人免疫球蛋白,10%)销售额实现了29%的强劲增长,HIZENTRA®(人皮下免疫球蛋白,20%)销售额增长12%。随着免疫缺陷、继发性免疫缺陷和慢性炎症性脱髓鞘性多发性神经病(CIDP)患者诊断率提升,公司免疫球蛋白业务有望持续增长。
4.3奥克特珐玛(OCTPHARMA):奥克特珐玛采浆量显著恢复,业绩加速增长
奥克特珐玛浆站超过170个,23年采浆量复苏,同时免疫球蛋白产品组合Fibryga®、Wilate®和Nuwiq®下游需求旺盛。23年公司收入32.7亿欧元(+14.4%),实现营业利润4.36亿欧元。23年公司完成了LEX-209的III期研究,研究了octaplex®(四因子凝血酶原复合物浓缩物)的有效性和安全性,octaplex®用于治疗接受维生素K拮抗剂抗凝治疗且需要紧急手术且出血风险显著的患者。