2024肺癌免疫治疗新进展报告
投资要点
依沃西单抗:两大临床引发NSCLC治疗变革
NSCLC是目前肿瘤免疫药物的必争之地,帕博利珠单抗凭借KEYNOTE系列研究奠定了NSCLC一线治疗领域的领先和“药王”地位。在近期的两个III期临床结果披露后,依沃西单抗已经全面展现了肺癌领域的BIC潜力:1)在HARMONi-2研究中在PD-L1 TPS≥ 1%的驱动基因阴性患者中头对头击败帕博利珠单抗;2)在HARMONi-A研究中针对EGFR-TKI耐药的患者获得了显著的PFS优势、OS获益的趋势和良好的安全性,综合收益较基于EGFR/c-MET双抗或PD-1/PD-L1单抗的方案更有竞争力。依沃西单抗于5月24日获NMPA批准上市,我们将其国内峰值销售额自66亿上调至71亿元,并关注其未来与ADC药物联用的机会。
另一方面,本次两个临床研究的成功强化了依沃西单抗海外临床的信心。目前公司的合作伙伴Summit Therapeutics在海外推进HARMONi(HARMONi-A的海外部分)和HARMONi-3两个III期临床研究,基于前者有望在下半年完成临床入组。公司步入2.0时代,预计2H24多个催化剂兑现公司正从biopharma向能自我造血的药企进化:1)卡度尼利单抗销售额的快速提升已经证实了公司强大的商业化能力;2)随着依沃西单抗的获批和伊努西单抗、依若奇单抗等的潜在获批,公司商业化产品线数量和质量有望进一步提升,有望驱动产品营收自2024年持续增长。我们预计公司在2025年实现盈利。
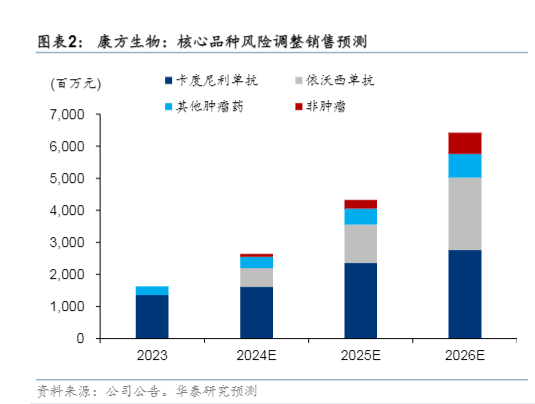
下半年公司有望迎来多个重磅催化:1)HARMONi-2研究的数据有望在WCLC披露结果;2)PCSK9单抗伊努西单抗和IL-12/23单抗依若奇单抗均有望在年内获批;3)IL-17单抗古莫奇单抗有望递交NDA;4)预计AK112-306研究和卡度尼利单抗的肝癌辅助治疗III期临床完成临床入组。
维持“买入”评级,给予目标价60.54港币
公司2021/2022/2023年营收2.26/8.38/45.26亿元,归母净利润(10.75)/(11.68)/20.28亿元,2023年营收和利润的大幅上涨主要源于来自SummitTherapeutics的依沃西单抗授权许可首付款。考虑到公司商业化的进展、依沃西单抗在头对头研究中的阳性结果和当前PD-1单抗领域的竞争格局,我们预计2024/2025/2026年公司营收为25.72/42.20/62.93亿元,归母净利润为(3.60)/3.77/10.30亿元,有望在2025年实现盈利。采用DCF方法,我们给予公司目标市值487亿元(基于9.3%的WACC和3.0%的永续增长率),对应目标价60.54港币,维持“买入”评级。与市场观点不同,我们认为公司的长期成长有非常明确的路径:1)公司已经验证了在国内市场的强执行力,如卡度尼利单抗上市第二年在无医保支付的情况下销售额破10亿元及HARMONi-2和HARMONi-A两个研究的快速推进,在竞争较为激烈的国内市场能够更好地把握先发优势;2)ADC药物在NSCLC领域同样进展显著,但其主要针对当前主流的化免方案的化疗端进行升级;依沃西单抗在验证了作为BIC IO药物的潜力后,有望持续优化化免方案的免疫端,其与ADC药物并非竞争关系,而更类似合作关系;我们已在后文列举了部分PD-1/PD-L1单抗和ADC联用方案治疗肺癌的进展,预计未来依沃西单抗亦将成为联合治疗的选择之一。
KEYNOTE系列研究:PD-1抗体称霸肺癌治疗的基石2023年,帕博利珠单抗以250.1亿美元的销售额登顶全球“药王”,核心因素之一是其在肺癌领域的绝对领先地位。根据Evaluate Pharma的数据,2020年帕博利珠单抗(Keytruda)全球收入143.80亿美元,其中53%来自NSCLC适应症。
帕博利珠单抗在肺癌领域的优势来自于其为患者带来的长期生存、去化疗等获益,并通过了高标准(如PFS/OS双终点)、长期随访结果带来的高级别循证医学证据的验证,其中最具代表性的便是默沙东开启的肺癌一线治疗的KEYNOTE系列临床研究。从该系列研究,我们可以看到IO在肺癌领域适应症不断拓展优化的过程。KEYNOTE-024:首次改写NSCLC治疗格局KEYNOTE-024研究是一项在PD-L1 TPS≥50%、无EGFR和ALK驱动基因突变晚期NSCLC患者中对照帕博利珠单抗单药和含铂化疗的III期临床研究。305名患者按1:1分组后,其中化疗组患者疾病进展后可交叉至帕博利珠单抗组。临床结果显示了帕博利珠单抗较化疗的显著患者获益:1)ORR(46.1% vs 31.1%)和PFS(7.7 vs 5.5月)均显著优于化疗组,7名试验组患者获得完全缓解(对照组为零);2)经长期随访,试验组取得了26.3 vs 13.4月的OS优势(HR = 0.62),5年OS率较化疗组提升近一倍(31.9%vs16.3%);3)帕博利珠单抗安全性良好,TRAE(76.7% vs 90.0%)和3级及以上TRAE(31.2% vs 53.3%)发生率明显低于化疗组。
KEYNOTE-024研究的意义在于:1)其首次以高标准的临床数据,证实了IO治疗在肺癌领域能够实现OS获益;2)在适当的肺癌患者人群中首次实现“无化疗”方案,带来更优的患者生存质量。KEYNOTE-042:IO单药适用人群扩展KEYNOTE-042研究扩大了研究样本,将PD-L1 TPS ≥ 1%的EGFR和ALK驱动基因阴性患者纳入临床,对比帕博利珠单抗单药和含铂化疗。1,274名患者按1:1分配至帕博利珠单抗和研究者选择的化疗方案组。5年的跟踪证实了帕博利珠单抗单药治疗在TPS ≥ 1%患者中的长期获益:1)与化疗相比,试验组取得了16.4 vs 12.1月(HR = 0.79)的显著OS优势;2)与KEYNOTE-024研究相似,KEYNOTE-042研究中的5年OS率同样较化疗组接近翻倍(16.6%vs8.5%);3)在中国患者人群及KEYNOTE-042中国扩展研究中,试验组较化疗组取得了20.2 vs 13.5月(HR = 0.66)的显著OS优势和19.0%vs9.5%的5年OS率领先。然而,亚组分析显示KEYNOTE-042研究中帕博利珠单抗组的患者获益主要来自TPS ≥ 50%的人群,TPS 1%~49%的患者OS的HR值在95%置信区间的上限超过1.0;TPS ≥ 1%患者的PFS为5.6 vs 6.8月(HR = 1.03),两组无显著性差异。
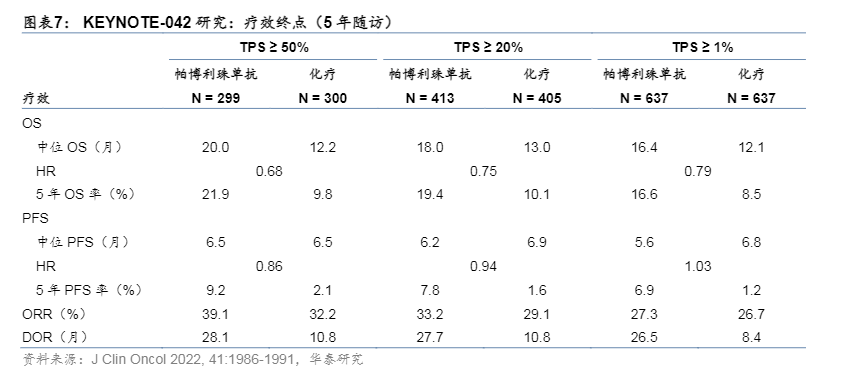
KEYNOTE-189:联合方案,人群扩张基于进一步将适用人群扩大的目的,默沙东启动了KEYNOTE-189研究,纳入616例不考虑初始PD-L1状态、EGFR和ALK驱动基因阴性非鳞NSCLC患者,探索帕博利珠单抗联合含铂化疗和单纯使用含铂化疗的差异。帕博利珠单抗和化疗的联用带来了显著的短期和长期患者获益:1)联用组的PFS达到9.0月,显著优于化疗组的4.9月(HR = 0.50);ORR达到48.3%,明显高于化疗组的19.9%;2)试验组的OS达到22.0月,显著优于对照组的10.6月(HR = 0.60);5年OS率为19.4% vs 11.3%,试验组明显领先;3)尤其对完成联合治疗后接受35个周期帕博利珠单抗单药维持治疗的57名患者,ORR达到86.0%(包括8例完全缓解),完成治疗后的3年OS率达到71.9%;4)与IO单药不同,联合方案在TPS 1%~49%和TPS < 1%的患者中均取得显著疗效,前者中试验组和对照组的PFS和OS分别为9.4vs 4.9月(HR = 0.57)和21.8vs 12.1月(HR = 0.65),后者的PFS和OS分别为6.2vs 5.1月(HR = 0.67)和17.2vs 10.2月(HR = 0.55)。
KEYNOTE-189研究首次将PD-1抗体的治疗范围推进至驱动基因阴性全人群,使得免疫治疗成为NSCLC一线治疗的首选方案。与此同时,该研究成为非鳞NSCLC一线治疗的经典临床设计,后续多款国产PD-1抗体均采用相似的设计完成了III期临床研究。KEYNOTE-407:填补鳞癌空白肺鳞癌的病理学与非鳞癌差异明显,异质性较强。KEYNOTE-407研究对比了帕博利珠单抗和安慰剂分别联合含铂化疗治疗肺鳞癌的疗效和安全性,合计559名患者按1:1随机分配至试验组和对照组。帕博利珠单抗和化疗的联用在鳞癌患者中同样带来显著获益:1)试验组的ORR(62.2% vs 38.8%)和PFS(8.0vs 5.1月)均显著优于化疗组;2)与化疗相比,试验组取得了17.2 vs 11.6月(HR = 0.71)的显著OS优势,5年OS率同样达到18.4% vs 9.7%的接近翻倍水准;3)57名完成联合治疗后接受35个周期帕博利珠单抗单药维持治疗的患者获得90.9%的ORR和16.4%的完全缓解,完成治疗后的3年OS率达到69.5%;4)中国亚组和中国扩展队列的125名患者中试验组取得了78.5% vs 41.7%的ORR优势、8.3 vs 4.2月(HR = 0.32)的PFS优势和17.3 vs 12.6月(HR = 0.44)的OS优势。
KEYNOTE-407研究将免疫治疗带入肺鳞癌领域,解决了鳞癌患者缺乏有效治疗手段的困境,并实现了PD-1抗体对非基因驱动型NSCLC患者的全覆盖。另一方面,中国患者积极参与该研究,为国产PD-1抗体的后续快速推进提供参考。
国产PD-1单抗梯队:参照KEYNOTE系列研究实现商业化截至6M24,已有9款PD-1/PD-L1单抗在国内获批用于NSCLC的一线治疗,其中7款为国产品种,获批用于一线NSCLC适应症对应的注册临床在设计方面均参考了对应的KEYNOTE系列研究,并证实了PD-1/PD-L1单抗和化疗联合方案带来的患者获益。但另一方面,不同PD-1/PD-L1单抗之间没有头对头研究,其中不存在真正意义上的best-in-class。
依沃西单抗:从头对头优效走向全球潜在重磅
在帕博利珠单抗在肺癌领域的临床研究基础上,康方生物的依沃西单抗更进一步,在TPS ≥ 1%和EGFR-TKI耐药的NSCLC患者中取得了更优疗效,展现了全球BIC的潜力,且未来有望作为化免联合方案中IO药物的升级版本,和ADC联用而带来更优的疗效。依沃西单抗已于2Q24在国内获批上市,商业化快速展开,我们预计其国内峰值销售额有望达到71亿元。
切入无人区,验证NSCLC全球BIC潜力如前文所述,帕博利珠单抗通过一系列临床研究奠定了在NSCLC一线治疗中的主导地位,此外亦通过KEYNOTE-010研究的结果在海外覆盖了PD-L1表达的NSCLC二线患者。依沃西单抗一方面通过头对头研究在TPS ≥ 1%的一线治疗患者击败前者,有望颠覆当前治疗格局,另一方面在帕博利珠单抗失败的EGFR-TKI耐药领域取得阳性结果,展现了依沃西单抗的全球BIC潜力。HARMONi-2(AK112-303):一鸣惊人,全球BIC起步II期临床初现强竞争力。依沃西单抗的II期AK112-202研究纳入了初始治疗的PD-L1阳性患者。公司披露的数据显示,截至6M23,合计66名患者接受了依沃西单抗单药治疗:1)ORR和DCR分别为68.3%和97.6%;2)中位PFS达到10.1月,6个月的PFS率达到66.1%;3)24个月的OS率达到61.2%。尽管并无头对头研究且研究规模相差甚远,但上述结果和KEYNOTE-042研究的肩对肩比较已充分展现了依沃西单抗的潜力。
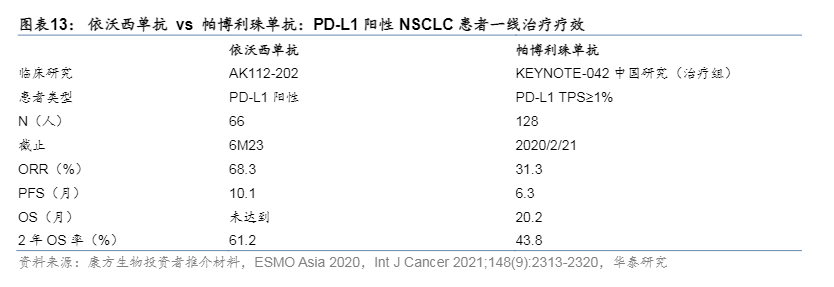
初步解构HARMONi-2:全方位优势。在II期临床基础上,公司启动了III期临床HARMONi-2(AK112-303)研究,头对头比较依沃西单抗和帕博利珠单抗的疗效。该研究招募398名驱动基因阴性、PD-L1阳性的NSCLC患者,于2022年11月FPI,并于2023年8月完成入组。5月31日,公司公告HARMONi-2研究取得阳性结果,依沃西单抗成为全球首个在III期临床中头对头击败帕博利珠单抗的品种。尽管目前尚无详细数据披露,我们认为从现有结果判断,依沃西单抗的临床价值已经充分展现,有效解决了帕博利珠单抗的不足:1)HARMONi-2研究纳入了占比57.8%的TPS 1%~49%患者,与KEYNOTE-042研究帕博利珠单抗组的53.1%相仿,与真实世界患者表达水平分布一致。如前文所述,KEYNOTE-042研究的结果显示帕博利珠单抗在TPS 1%~49%的患者中疗效有限,患者获益主要来自TPS ≥ 50%的人群,而HARMONi-2研究显示依沃西单抗在前者中亦取得了显著的PFS获益。2)KEYNOTE-042研究中,帕博利珠单抗单药和对照组的PFS曲线在早期交叉,或因PD-1单抗在早期起效慢于化疗,治疗前期获益较少,继而导致TPS≥1%患者的PFS不显著(HR=1.07)。依沃西单抗在TPS 1%~49%的患者中取得PFS获益,有望带来更优的早期疗效。
初步展现后续临床潜力。此外,我们认为HARMONi-2研究的现有结果进一步验证了依沃西单抗的后续临床—尤其是海外临床的潜力:1)依沃西单抗在不同亚组均有PFS强获益,其中包括鳞癌亚组;考虑到目前主要的抗血管生成药物贝伐珠单抗不可用于鳞癌治疗,依沃西单抗在肺鳞癌中的疗效和安全性更显突破性。目前依沃西单抗与替雷利珠单抗头对头的AK112-303研究和与帕博利珠单抗头对头的HARMONi-3海外研究均在鳞癌患者中展开,我们认为其已在鳞癌患者中取得的进展有望进一步映射至上述两项研究。2)即使在帕博利珠单抗的优势人群(TPS ≥ 50%),依沃西单抗同样获得优效;叠加TPS 1%~49%人群中的获益,我们认为依沃西单抗的疗效优势有望进一步延伸到全人群,HARMONi-3研究的潜力较大,依沃西单抗在美国市场的竞争优势有望进一步放大。HARMONi-A(AK112-301):冲击难治后线,初战告捷EGFR-TKI耐药NSCLC:方案寥寥。EGFR-TKI是EGFR突变NSCLC患者的基础治疗方案,目前一线应用三代EGFR-TKI已可将PFS提升至18.9~22.1月(参考FLAURA、AENEAS、FURLONG、IBIO-103等研究)。然而,三代EGFR-TKI耐药后机制复杂,后续治疗方案有限,化疗和抗血管生成药物是通常的选择。IO屡败屡战。
免疫治疗在驱动基因阴性NSCLC患者中已成为基石疗法,但在三代EGFR-TKI耐药患者中屡屡碰壁:1)纳武利尤单抗的III期CheckMate 722研究显示,其联合化疗较化疗组的PFS为5.6 vs 5.4月(HR = 0.75),OS为19.4 vs 15.9月(HR = 0.82),均无显著差异;2)帕博利珠单抗的KEYNOTE-789研究显示,其联合化疗较化疗组的PFS为5.6 vs 5.5月(HR = 0.80),OS为15.9 vs 14.7月(HR = 0.84),均未达到显著;3)阿替利珠单抗联合贝伐珠单抗和含铂双药的四药方案在中国III期临床IMpower151研究中较贝伐珠单抗和化疗的联合方案未能带来PFS改善(8.5 vs 8.3月),同样方案在韩国进行的ATTLAS研究展现了较化疗的PFS获益,但OS无差异;4)信迪利单抗联合贝伐珠单抗和化疗的方案在ORIENT-31中取得了PFS获益,并借此获批上市,成为首个获监管机构认可的方案。
依沃西单抗:弄潮儿向涛头立。HARMONi-A(AK112-301)III期临床招募了322名EGFR-TKI耐药的NSCLC患者,比较依沃西单抗和安慰剂分别联合培美曲塞和卡铂的疗效。2024年6月,公司在ASCO披露了本研究的阳性结果:1)试验组的PFS显著优于对照组(7.1 vs 4.8月,HR = 0.46),6个月和9个月的PFS率分别为55.4% vs 33.1%和37.9% vs 18.3%;2)试验组的反应率更高,ORR和DCR分别为50.6% vs 35.4%和93.1% vs 83.2%;3)数据成熟度到达52%时,试验组的OS呈现获益趋势(17.1 vs 14.5月,HR = 0.80),且试验组的OS仍有望继续延长,12月的OS率为65.4% vs 59.8%;4)脑转移、T790M阳性等亚组均展现和总人群一致的显著PFS获益;5)安全性可控,3级及以上TRAE发生率54.0%,不良事件主要以血液学毒性为主,与化疗相关。
(本文仅供参考,不代表我们的任何投资建议。如需使用相关信息,请参阅报告原文。)